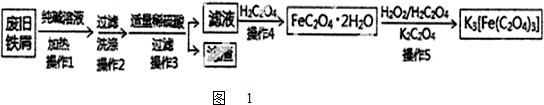
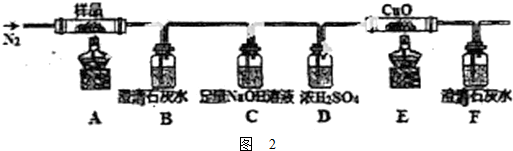
题目内容
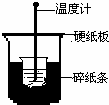 50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在下图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在下图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:(1)从实验装置上看,图中尚缺少的一种玻璃用品是
(2)烧杯间填满碎纸条的作用是
(3)大烧杯上如不盖硬纸板,求得的中和热数值将
(4)实验中改用60mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液进行反应,与上述实验相比较,所放出的热量
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得中和热的数值与57.3kJ/mol相比较会
(6)该实验装置中有一个明显的错误是:
考点:中和热的测定
专题:实验题
分析:(1)根据量热计的构造来判断该装置的缺少仪器;
(2)中和热测定实验成败的关键是保温工作;
(3)不盖硬纸板,会有一部分热量散失;
(4)反应放出的热量和所用酸以及碱的量的多少有关,并根据中和热的概念和实质来回答;
(5)根据弱电解质电离吸热分析;
(6)小烧杯口应与大烧杯口相平.
(2)中和热测定实验成败的关键是保温工作;
(3)不盖硬纸板,会有一部分热量散失;
(4)反应放出的热量和所用酸以及碱的量的多少有关,并根据中和热的概念和实质来回答;
(5)根据弱电解质电离吸热分析;
(6)小烧杯口应与大烧杯口相平.
解答:
解:(1)根据量热计的构造可知该装置的缺少仪器是环形玻璃搅拌器,故答案为:环形玻璃搅拌器;
(2)中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎纸条的作用是:减少实验过程中的热量损失,故答案为:减少实验过程中的热量损失;
(3))大烧杯上如不盖硬纸板,会有一部分热量散失,求得的中和热数值将会减小,故答案为:偏小;
(4)反应放出的热量和所用酸以及碱的量的多少有关,并若用60mL0.25mol?L-1H2SO4溶液跟50mL0.55mol?L-1NaOH溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高,但是中和热的均是强酸和强碱反应生成1mol水时放出的热,与酸碱的用量无关,所以用50mL0.50mol?L-1盐酸代替H2SO4溶液进行上述实验,测得中和热数值相等,故答案为:不相等;相等;因为中和热是指酸跟碱发生中和反应生成1molH2O所放出的热量,与酸碱的用量无关;
(5)氨水为弱碱,电离过程为吸热过程,所以用氨水代替稀氢氧化钠溶液反应,反应放出的热量偏小,求得的中和热数值将会减小,故答案为:偏小;
(6)由图可知小烧杯口没有与大烧杯口相平,故答案为:小烧杯口没有与大烧杯口相平.
(2)中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎纸条的作用是:减少实验过程中的热量损失,故答案为:减少实验过程中的热量损失;
(3))大烧杯上如不盖硬纸板,会有一部分热量散失,求得的中和热数值将会减小,故答案为:偏小;
(4)反应放出的热量和所用酸以及碱的量的多少有关,并若用60mL0.25mol?L-1H2SO4溶液跟50mL0.55mol?L-1NaOH溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高,但是中和热的均是强酸和强碱反应生成1mol水时放出的热,与酸碱的用量无关,所以用50mL0.50mol?L-1盐酸代替H2SO4溶液进行上述实验,测得中和热数值相等,故答案为:不相等;相等;因为中和热是指酸跟碱发生中和反应生成1molH2O所放出的热量,与酸碱的用量无关;
(5)氨水为弱碱,电离过程为吸热过程,所以用氨水代替稀氢氧化钠溶液反应,反应放出的热量偏小,求得的中和热数值将会减小,故答案为:偏小;
(6)由图可知小烧杯口没有与大烧杯口相平,故答案为:小烧杯口没有与大烧杯口相平.
点评:本题考查中和热的测定,题目难度中等,注意理解中和热的概念和测定原理是解题的关键.

练习册系列答案
相关题目
下列实验可实现鉴别目的是( )
| A、用BaCl2溶液鉴别SO3(g)和SO2 |
| B、用Ca(OH)2溶液鉴别Na2CO3溶液和NaHCO3溶液 |
| C、用CO2鉴别NaAlO2溶液和Na2SiO3溶液 |
| D、用湿润的碘化钾淀粉试纸鉴别Br2(g)和NO2 |
水溶液X中只可能溶有K+、Ca2+、AlO2-、SiO32-、CO32-、SO42-中的若干种离子.某同学对该溶有进行了如下实验下列判断正确的是( )


| A、气体甲一定是纯净物 |
| B、沉淀甲是硅酸和硅酸钙的混合物 |
| C、K+、AlO2-、SiO32-、和CO32-一定存在于溶液X中 |
| D、SO42-一定不存在于溶液X中 |
下列物质的分离方法不正确的是( )
| A、用过滤的方法除去食盐中泥沙 |
| B、用蒸馏的方法将海水淡化 |
| C、用酒精萃取碘水中的碘单质 |
| D、用加热的方法除去碳酸钠中的碳酸氢钠 |
有关AgCl沉淀的溶解平衡说法正确的是( )
| A、AgCl沉淀生成和沉淀溶解不断进行,但速率相等 |
| B、AgCl难溶于水,溶液中没有Ag+和Cl- |
| C、在AgCl的澄清饱和溶液中,只要向其中加入NaCl溶液,一定会有沉淀生成 |
| D、向含有AgCl沉淀的悬浊液中加入NaCl固体,AgCl的溶解度增大 |