题目内容
12.下列各组中的X和Y两种原子,化学性质一定相似的是( )| A. | X原子和Y原子最外层都只有一个电子 | |
| B. | X原子2p能级上有三个电子,Y原子的3p能级上有三个电子 | |
| C. | X原子的核外电子排布为1s2,Y原子的核外电子排布为1s22s2 | |
| D. | X原子核外M层上仅有两个电子,Y原子核外N层上仅有两个电子 |
分析 A.如H和Na原子最外层都只有1个电子性质不同;
B.X为N,Y为P;
C.X为He,Y为Be;
D.X为Mg,Y的M层电子数不确定.
解答 解:A.X原子和Y原子最外层都只有一个电子,如H和Na最外层都只有1个电子性质不同,故A错误;
B.X为N,Y为P,同主族元素,其化学性质相似,故B正确;
C.X为He,属于稀有气体,化学性质不活泼,Y为Be,属于金属元素,化学性质较活泼,二者性质不同,故C错误;
D.X为Mg,Y的M层电子数不确定,满足N层上仅有两个电子的元素有多种,故D错误.
故选B.
点评 本题考查原子结构与元素的性质,注意把握元素原子的电子排布式,侧重于基础知识的考查,题目难度不大,侧重于考查学生的分析能力和对基础知识的应用能力.

练习册系列答案
相关题目
2.表给出了14种元素的电负性.
已知:两成键元素间电负性差值大于1.7时,形成离子键;两成键元素间电负性差值小于1.7时,形成共价键.
(1)根据表中给出的数据,可推知元素的电负性具有的变化规律是在同一周期中,随着原子序数的递增,元素的电负性逐渐增大,并呈周期性变化;.
(2)判断下列物质是离子化合物还是共价化合物.
Mg3N2:离子化合物;BeCl2:共价化合物;AlCl3:共价化合物;SiC:共价化合物.
| 元素 | Al | B | Be | C | Cl | F | Li |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 |
| 元素 | Mg | N | Na | O | P | S | Si |
| 电负性 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
(1)根据表中给出的数据,可推知元素的电负性具有的变化规律是在同一周期中,随着原子序数的递增,元素的电负性逐渐增大,并呈周期性变化;.
(2)判断下列物质是离子化合物还是共价化合物.
Mg3N2:离子化合物;BeCl2:共价化合物;AlCl3:共价化合物;SiC:共价化合物.
3.下列事实能判断金属元素甲的金属性一定比乙强的有( )
①甲单质能与乙盐的溶液反应并置换出乙
②甲、乙两元素原子的最外层电子数相同,且甲的原子半径小于乙
③甲、乙两短周期元素原子的电子层数相同,且甲的原子序数小于乙
④甲、乙两元素的最高价氧化物水化物的碱性甲大于乙.
①甲单质能与乙盐的溶液反应并置换出乙
②甲、乙两元素原子的最外层电子数相同,且甲的原子半径小于乙
③甲、乙两短周期元素原子的电子层数相同,且甲的原子序数小于乙
④甲、乙两元素的最高价氧化物水化物的碱性甲大于乙.
| A. | 全部可以 | B. | 仅②可以 | C. | 仅②③可以 | D. | ①③④可以 |
20.下列离子方程式错误的是( )
| A. | 向硫酸氢钠溶液中滴加氢氧化钡溶液:Ba2++2OH-+2H++SO42-=BaS04↓+2H2O | |
| B. | 酸性介质中KMnO4氧化 H2O2:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O | |
| C. | NaClO溶液中通入过量SO2:ClO-+SO2+H2O=HClO+HS03- | |
| D. | 向明矾溶液中滴加少量Ba(OH)22Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ |
1.有机物的结构可用“键线式”表示,如:CH3CH=CHCH3可简写为 .有机物X的键线式为
.有机物X的键线式为 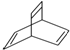 ,下列说法正确的是( )
,下列说法正确的是( )
 .有机物X的键线式为
.有机物X的键线式为  ,下列说法正确的是( )
,下列说法正确的是( )| A. | X的化学式为C8H10 | |
| B. | 有机物Y  与X互为同系物 与X互为同系物 | |
| C. | X因发生加成反应而使酸性高锰酸钾溶液褪色 | |
| D. | X与足量的H2在一定条件下反应可生成环状烃Z,Z的一氯代物有2种 |
2.下列化学用语正确的是( )
| A. | 硫化氢分子的电子式: | B. | S2-的结构示意图: | ||
| C. | HClO的结构式:H-O-Cl | D. | NH4Cl的电子式: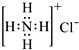 |