题目内容
生活中处处有化学,下列表述不正确的是( )
| A、对不可回收的垃圾常用的处理方法有卫生填埋、堆肥和焚烧 |
| B、制造玻璃是复杂的物理变化,玻璃的组成不同,性能也不同 |
| C、血糖过低的患者可利用静脉注射葡萄糖溶液的方法迅速补充营养 |
| D、固体煤经处理变为气体燃料后,可以减少SO2和烟尘的污染,且燃烧效率高 |
考点:常见的生活环境的污染及治理,玻璃的主要化学成分、生产原料及其用途,药物的主要成分和疗效
专题:化学应用
分析:A.对环境不产生污染的垃圾可卫生掩埋、堆肥;
B.二氧化硅与碳酸钠、碳酸钙是制造玻璃的原料;
C.静脉注射葡萄糖溶液可以补充能量;
D.煤经处理变为气体燃料后,燃烧更加充分,能量利用率更高,可以减少有害和烟尘的排放.
B.二氧化硅与碳酸钠、碳酸钙是制造玻璃的原料;
C.静脉注射葡萄糖溶液可以补充能量;
D.煤经处理变为气体燃料后,燃烧更加充分,能量利用率更高,可以减少有害和烟尘的排放.
解答:
解:A.对环境不产生污染的垃圾可卫生掩埋、堆肥,有些垃圾可焚烧,但产生污染性气体的垃圾不能焚烧,故A正确;
B.二氧化硅与碳酸钠、碳酸钙是制造玻璃的原料,二氧化硅与碳酸钠、碳酸钙能发生化学反应,故B错误;
C.静脉注射葡萄糖溶液可以迅速补充能量,故C正确;
D.煤经处理变为气体燃料后,燃烧更加充分,提高了燃烧效率,能量利用率更高,可以减少有害和烟尘的排放,有利于“节能减排”,故D正确.
故选B.
B.二氧化硅与碳酸钠、碳酸钙是制造玻璃的原料,二氧化硅与碳酸钠、碳酸钙能发生化学反应,故B错误;
C.静脉注射葡萄糖溶液可以迅速补充能量,故C正确;
D.煤经处理变为气体燃料后,燃烧更加充分,提高了燃烧效率,能量利用率更高,可以减少有害和烟尘的排放,有利于“节能减排”,故D正确.
故选B.
点评:本题考查了能源的利用与环境保护、玻璃的成分等生产生活中常见问题,难度不大,注意积累.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
原子序数大于4的主族元素X、Y的离子Xm+、Yn-的核外电子排布相同,关于X、Y 元素的论述正确的是( )
| A、X原子半径小于Y |
| B、X和Y的核电荷数之差为m-n |
| C、电负性X>Y |
| D、第一电离能 X<Y |
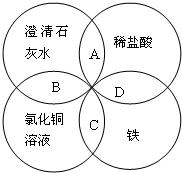 铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中常见物质,四种物质间的反应关系如图所示.图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应反应的离子方程式书写正确的是( )
铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中常见物质,四种物质间的反应关系如图所示.图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应反应的离子方程式书写正确的是( )| A、OH-+HCl=H2O+Cl- |
| B、Ca(OH)2+Cu2+=Ca2++Cu(OH)2↓ |
| C、Fe+Cu2+=Cu+Fe2+ |
| D、Fe+2H+=Fe3++H2↑ |
用铝箔包裹着2.3克金属钠投入到足量水中,理论上可以收集到氢气物质的量为( )
| A、0.05mol |
| B、0.2mol |
| C、大于0.05mol小于等于0.2mol |
| D、无法判断 |
下列化学用语中,书写正确的是( )
| A、乙烯的结构简式:CH2CH2 |
| B、氮气的结构式:N≡N |
C、水分子的电子式: |
D、硫原子的结构示意图: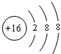 |
能证明硅酸的酸性弱于碳酸酸性的实验事实是( )
| A、CO2溶于水形成碳酸,SiO2难溶于水 |
| B、CO2通入可溶性硅酸盐中析出硅酸沉淀 |
| C、高温下SiO2与碳酸盐反应生成CO2 |
| D、HCl通入可溶性碳酸盐溶液中放出气体,氯化氢通入可溶性硅酸盐溶液中生成沉淀 |
下列说法正确的是( )
| A、测定HCl和NaOH反应的中和热时,每次实验均应测量3个温度,即盐酸起始温度、NaOH起始温度和反应后终止温度 |
| B、在101 kPa时,1 mol H2完全燃烧生成液态水,放出285.8 kJ热量,H2的燃烧热为:-285.8kJ?mol-1 |
| C、在101 kPa时,1 mol C与适量O2反应生成1 mol CO时,放出110.5 kJ热量,则C的燃烧热为110.5 kJ?mol-1 |
| D、生成物总能量一定低于反应物总能量,同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同 |
