题目内容
下面是某同学探究Na2O2性质过程中的一个片段.请你帮助他补全活动记录.
【观察】Na2O2的颜色、状态 色; 态.
【预测】从组成上分析,Na2O2为金属氧化物,可能会跟二氧化碳、水等反应,生成盐.
【实验】
【由现象推出结论】
写出溶液中发生反应的离子方程式:
经测定,反应后在铁丝网上的白色固体与开始时加入烧杯中的粉末状物质组成完全相同.请写出铁丝网上反应的化学方程式: .
【观察】Na2O2的颜色、状态
【预测】从组成上分析,Na2O2为金属氧化物,可能会跟二氧化碳、水等反应,生成盐.
【实验】
| 实验内容 | 实验现象(填入下栏) |
如右图,在一个100ml烧杯中,加入3~4药匙Na2CO3,粉末,用一张比烧杯口稍大,中部呈凹形的铁丝网,凹部放入疏松的脱脂棉包裹着的过氧化钠,向烧杯中加入适量3mol?L-1盐酸,立即把铁丝网放在烧杯上.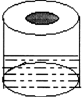 |
写出溶液中发生反应的离子方程式:
经测定,反应后在铁丝网上的白色固体与开始时加入烧杯中的粉末状物质组成完全相同.请写出铁丝网上反应的化学方程式:
考点:性质实验方案的设计,钠的重要化合物
专题:实验设计题
分析:过氧化钠是淡黄色的固体,碳酸钠可以和盐酸反应生成氯化钠、水以及二氧化碳气体,过氧化钠可以和二氧化碳反应生成碳酸钠和氧气,反应放热并且生成的氧气具有助燃性,据此回答.
解答:
解:过氧化钠是淡黄色的固体,向碳酸钠中滴加盐酸,碳酸钠可以和盐酸反应生成氯化钠、水以及二氧化碳气,即CO32-+2H+=H2O+CO2↑,过氧化钠可以和二氧化碳反应生成白色固体碳酸钠和氧气,即2Na2O2+2CO2=2Na2CO3+O2,反应放热并且生成的氧气具有助燃性,所以脱脂棉燃烧起来,
故答案为:淡黄;固;烧杯中有大量气体生成,脱脂棉迅速燃烧,铁丝网上有白色固体,烧杯中Na2CO3与盐酸反应生成CO2气体,Na2O2与CO2反应放热并有O2生成,引燃脱脂棉;CO32-+2H+=H2O+CO2↑;2Na2O2+2CO2=2Na2CO3+O2.
故答案为:淡黄;固;烧杯中有大量气体生成,脱脂棉迅速燃烧,铁丝网上有白色固体,烧杯中Na2CO3与盐酸反应生成CO2气体,Na2O2与CO2反应放热并有O2生成,引燃脱脂棉;CO32-+2H+=H2O+CO2↑;2Na2O2+2CO2=2Na2CO3+O2.
点评:本题考查学生过氧化钠和碳酸钠的化学性质,注意知识的归纳和梳理是解题的关键,难度不大.

练习册系列答案
相关题目
浓度均为0.1mol.L-1的Na2CO3和盐酸各0.5L,有甲乙两位同学进行实验,甲向Na2CO3溶液中滴加盐酸至完全反应乙向盐酸中滴加Na2CO3至完全反应.两位同学在实验过程中产生的CO2气体比较结果正确的是( )
| A、甲>乙 | B、甲<乙 |
| C、甲=乙 | D、无法确定 |
农药波尔多液不能用铁制容器盛放,是因为铁能与该农药中的硫酸铜起反应.该反应中,铁是( )
| A、氧化剂 | B、被还原 |
| C、还原剂 | D、氧化产物 |
某未知溶液中加入AgNO3溶液有白色沉淀生成,加入稀硝酸后,沉淀部分溶解,有无色无味的气体生成,将气体通入澄清石灰水中,石灰水变浑浊,已知该溶液中含有阴离子是如下四组中的一组.则它是( )
| A、Cl- SO42- |
| B、Cl- NO3- |
| C、Cl- CO32- |
| D、Cl- OH- |
常温常压下能大量共存,并可用浓硫酸干燥的一组气体是( )
| A、SO2、H2S、Cl2 |
| B、O2、CO2、NO |
| C、O2、H2、SO2 |
| D、NH3、N2、HCl |
将20.8g两种金属的混合物投入足量的盐酸中,反应完全后得到标准状况下氢气11.2L,该混合物的组成可能是( )
| A、铜和锌 | B、镁和铜 |
| C、铝和镁 | D、锌和铁 |
进行一氯取代反应后,只能生成三种沸点不同的有机物的烷烃是( )
| A、(CH3)2CHCH2CH2CH3 |
| B、(CH3CH2)2CHCH3 |
| C、(CH3)3CCH2CH3 |
| D、(CH3)2CHCH(CH3)2 |