题目内容
7.固体A的化学式为NH5,它的所有原子的最外层都符合相应稀有气体原子的最外电子层结构,则下列有关说法中,不正确的是( )| A. | 1mol NH5中含有5 mol N-H 键 | |
| B. | NH5的熔沸点高于NH3 | |
| C. | NH5固体投入少量水中,可产生两种气体 | |
| D. | NH5中既有离子键又有共价键 |
分析 固体A的化学式为NH5,它的所有原子的最外层都符合相应稀有气体原子的最外电子层结构,应为NH4H,是一种离子化合物,能与水反应:NH4H+H2O=NH3•H2O+H2↑,有氨气生成,以此来解答.
解答 解:A.根据氮原子的原子结构,最外层5个电子最多和四个氢原子形成共价键(其中一个是配位键,氮原子提供一对电子,氢离子提供空轨道形成),形成了带正电荷的铵根离子,所以另一个氢原子只能是形成H-,阴阳离子间形成离子键,故A错误;
B.NH4H是一种离子化合物,熔、沸点高于NH3,故B正确;
C.能与水反应:NH4H+H2O=NH3•H2O+H2↑,有氨气、氢气生成,故C正确;
D.NH5是离子化合物氢化铵,铵根中的氮原子与四个氢原子形成四个共价键,NH4+与H-之间为离子键,故D正确;
故选A.
点评 本题考查化学键,为高频考点,把握化学键形成的一般规律及化学键的判断为解答的关键,侧重分析与应用能力的考查,注意NH5为离子化合物,题目难度不大.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
15. 胡椒酚是植物挥发油中的一种成分,其结构简式如图.关于胡椒酚的下列说法:
胡椒酚是植物挥发油中的一种成分,其结构简式如图.关于胡椒酚的下列说法:
①该化合物属于芳香烃;②分子中至少有7个碳原子处于同一平面;
③它的部分同分异构体能发生银镜反应;
④该化合物的化学式为C9H11O.其中正确的是( )
 胡椒酚是植物挥发油中的一种成分,其结构简式如图.关于胡椒酚的下列说法:
胡椒酚是植物挥发油中的一种成分,其结构简式如图.关于胡椒酚的下列说法:①该化合物属于芳香烃;②分子中至少有7个碳原子处于同一平面;
③它的部分同分异构体能发生银镜反应;
④该化合物的化学式为C9H11O.其中正确的是( )
| A. | ①③ | B. | ①②④ | C. | ②③④ | D. | ②③ |
2.下列关于物质结构的说法中正确的是( )
| A. | BF3、HClO分子中所有原子都满足最外层8电子结构 | |
| B. | 某元素原子最外层电子数是次外层电子数的a(a为整数)倍,则该原子核内质子数为2a+2 | |
| C. | D2O分子与H2O分子是所含电子总数不相等的分子 | |
| D. | 在任何物质分子中都含有化学键 |
12.下列分子中所有碳原子不可能处在同一平面上的是( )
| A. |  | B. | 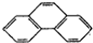 | C. |  | D. |  |
19.通常人们把拆开1mol某化学键吸收的能量看成该化学键的键能.键能的大小可以衡量化学键的强弱,也可以估计化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差.下列是一些化学键的键能
根据键能数据估算下列反应的反应热△H为:CH4 (g)+4F2 (g)═CF4(g)+4HF(g)( )
| 化学键 | C-H | C-F | H-F | F-F |
| 键能/(kJ•mol-1) | 414 | 489 | 565 | 155 |
| A. | -1940 kJ•mol-1 | B. | 1940 kJ•mol-1 | C. | -485 kJ•mol-1 | D. | 485 kJ•mol-1 |
16.下列有关叙述错误的是( )
| A. | 苯、甲苯、邻二甲苯、间二甲苯,它们之间都属于同系物 | |
| B. | 为了延长花果的成熟期,可用浸泡过高锰酸钾溶液的硅土吸收水果或花朵产生的乙烯 | |
| C. | 反应2CH3CHO+O2→2CH3COOH的原子利用率为100%,符合绿色化学理念 | |
| D. | 乙烯分子的球棍模型为: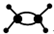 |
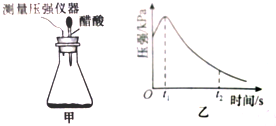
17.某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图甲).从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化.
 (1)上表中编号②实验中铁粉的质量为2.0g;编号③试验的实验目的是探究碳粉的质量对化学反应速率的影响
(1)上表中编号②实验中铁粉的质量为2.0g;编号③试验的实验目的是探究碳粉的质量对化学反应速率的影响
..
(2)编号①试验测得容器中压强随时间变化如图乙.t2时,容器中压强明显小于起始压强,其原因是铁发生了吸氧腐蚀,此时,碳粉表面发生了还原(填“氧化”或“还原”)反应,其电极反应式为O2+2H2O+4e-═4OH-.
(3)该小组对图乙中0~t1时压强增大的原因提出了如下假设:
假设一:发生析氢腐蚀产生了气体
假设二:反应开始时放热,导致容器温度升高,压强增大.
| 编号 | 实验目的 | 碳粉/g | 铁粉/g | 醋酸/% |
| ① | 为以下实验做参照 | 0.5 | 2.0 | 90.0 |
| ② | 探究醋酸浓度的影响 | 0.5 | 36.0 | |
| ③ | 0.2 | 2.0 | 90.0 |
 (1)上表中编号②实验中铁粉的质量为2.0g;编号③试验的实验目的是探究碳粉的质量对化学反应速率的影响
(1)上表中编号②实验中铁粉的质量为2.0g;编号③试验的实验目的是探究碳粉的质量对化学反应速率的影响..
(2)编号①试验测得容器中压强随时间变化如图乙.t2时,容器中压强明显小于起始压强,其原因是铁发生了吸氧腐蚀,此时,碳粉表面发生了还原(填“氧化”或“还原”)反应,其电极反应式为O2+2H2O+4e-═4OH-.
(3)该小组对图乙中0~t1时压强增大的原因提出了如下假设:
假设一:发生析氢腐蚀产生了气体
假设二:反应开始时放热,导致容器温度升高,压强增大.

