题目内容
(1)写出铝和氧化铁反应的化学方程式 ,并用双线桥法表示电子的转移情况
(2)写出下列反应的离子方程式
碳酸氢钠溶液与盐酸反应
碳酸氢钠溶液与氢氧化钠反应
氢氧化铝与盐酸反应
氢氧化铝与氢氧化钠反应
(3)写出下列反应的化学方程式
Ba2++SO42-=BaSO4↓ .
(2)写出下列反应的离子方程式
碳酸氢钠溶液与盐酸反应
碳酸氢钠溶液与氢氧化钠反应
氢氧化铝与盐酸反应
氢氧化铝与氢氧化钠反应
(3)写出下列反应的化学方程式
Ba2++SO42-=BaSO4↓
考点:离子方程式的书写,化学方程式的书写,氧化还原反应的电子转移数目计算
专题:氧化还原反应专题,离子反应专题
分析:(1)Al在高温下与氧化铁反应生成氧化铝和铁,反应中铝为还原剂、氧化铁为氧化剂,铝失去6个电子、铁离子得到得到6个电子;
(2)碳酸氢钠与盐酸反应生成氯化钠、二氧化碳气体和水;
碳酸氢钠与氢氧化钠反应生成碳酸钠和水;
氢氧化铝与盐酸反应生成氯化铝和水;
氢氧化铝与氢氧化钠反应生成偏铝酸钠和水;
(3)可溶性钡盐和可溶性硫酸盐生成硫酸钡和可溶性盐的离子反应为Ba2++SO42-=BaSO4↓.
(2)碳酸氢钠与盐酸反应生成氯化钠、二氧化碳气体和水;
碳酸氢钠与氢氧化钠反应生成碳酸钠和水;
氢氧化铝与盐酸反应生成氯化铝和水;
氢氧化铝与氢氧化钠反应生成偏铝酸钠和水;
(3)可溶性钡盐和可溶性硫酸盐生成硫酸钡和可溶性盐的离子反应为Ba2++SO42-=BaSO4↓.
解答:
解:(1)在高温条件下,铝和氧化铁发生氧化还原反应生成铁和氧化铝,电子转移的方向和数目可表示为: ,反应中铝为还原剂,并放出大量的热,可用于冶炼难熔金属,
,反应中铝为还原剂,并放出大量的热,可用于冶炼难熔金属,
故答案为: ;
;
(2)反应生成氯化钠、水和二氧化碳,离子反应为:H++HCO3-=H2O+CO2↑;
碳酸氢钠溶液与氢氧化钠溶液混合,反应生成碳酸钠和水,离子反应为:HCO3-+OH-=H2O+CO32-;
氢氧化铝与盐酸反应生成氯化铝和水,离子方程方程式为:Al(OH)3+3H+=Al3++3H2O;
氢氧化铝与氢氧化钠反应生成偏铝酸钠和水,离子方程方程式为:OH-+Al(OH)3=AlO2-+2H2O,
故答案为:H++HCO3-=H2O+CO2↑;HCO3-+OH-=H2O+CO32-;Al(OH)3+3H+=Al3++3H2O;OH-+Al(OH)3=AlO2-+2H2O;
(3)可溶性钡盐和可溶性硫酸盐生成硫酸钡和可溶性盐的离子反应为Ba2++SO42-=BaSO4↓,如:BaCl2+Na2SO4=BaSO4↓+2NaCl,
故答案为:BaCl2+Na2SO4=BaSO4↓+2NaCl.
 ,反应中铝为还原剂,并放出大量的热,可用于冶炼难熔金属,
,反应中铝为还原剂,并放出大量的热,可用于冶炼难熔金属,故答案为:
 ;
;(2)反应生成氯化钠、水和二氧化碳,离子反应为:H++HCO3-=H2O+CO2↑;
碳酸氢钠溶液与氢氧化钠溶液混合,反应生成碳酸钠和水,离子反应为:HCO3-+OH-=H2O+CO32-;
氢氧化铝与盐酸反应生成氯化铝和水,离子方程方程式为:Al(OH)3+3H+=Al3++3H2O;
氢氧化铝与氢氧化钠反应生成偏铝酸钠和水,离子方程方程式为:OH-+Al(OH)3=AlO2-+2H2O,
故答案为:H++HCO3-=H2O+CO2↑;HCO3-+OH-=H2O+CO32-;Al(OH)3+3H+=Al3++3H2O;OH-+Al(OH)3=AlO2-+2H2O;
(3)可溶性钡盐和可溶性硫酸盐生成硫酸钡和可溶性盐的离子反应为Ba2++SO42-=BaSO4↓,如:BaCl2+Na2SO4=BaSO4↓+2NaCl,
故答案为:BaCl2+Na2SO4=BaSO4↓+2NaCl.
点评:本题考查了化学方程式、离子方程式的书写、双线桥法表示氧化还原反应,题目难度中等,试题知识点较多,充分考查了学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
下列图示与对应的叙述相符的是( )
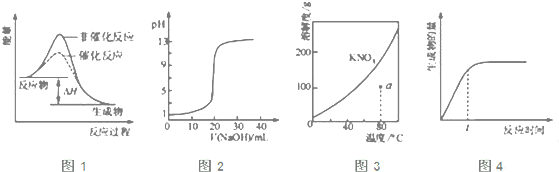

| A、图1表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
| B、图2表示0.1000 mol?L-1NaOH溶液滴定20.00mL0.1000 mol?L-1CH3COOH溶液所得到的滴定曲线 |
| C、图3表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液 |
| D、图4表示某可逆反应生成物的量随反应时间变化的曲线,由图知t时v正<v逆 |
将质量分数为a%的NaOH溶液蒸发掉mg水后,变成VmL2a%的NaOH不饱和溶液,则蒸发后的溶液的物质的量浓度是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列电离方程式正确的是( )
| A、NaHS溶于水:NaHS═Na++HS-,HS-+H2O?H3O++S2- |
| B、KH2PO4溶于水:H2PO4-?2H++PO43- |
| C、HF溶于水:HF═H++F- |
| D、NH4Cl溶于水:NH4++2H2O?NH3?H2O+H3O+ |
在同温同压条件下,物质的量相同的N2气体与H2气体之间的关系不正确的是( )
| A、体积都是22.4L |
| B、具有相同的体积 |
| C、具有相同的原子数 |
| D、具有相同的分子数 |
对1mol?L-1的MgCl2溶液的有关叙述中,正确的是( )
| A、该溶液中Cl-浓度为2 mol?L-1 |
| B、该溶液中Mg2+的物质的量是1 mol |
| C、可使用250 mL容量瓶分两次完成490 mL该浓度的MgCl2溶液的配制 |
| D、该溶液可由95g MgCl2?6H2O固体在水中溶解并稀释至1L获得 |
