题目内容
(1)标准状况下,112mL某气体的质量为0.14g,则其相对分子质量为 .
(2)1.56g可以显+1价的某金属与足量盐酸完全反应,生成0.04g氢气,则该金属的摩尔质量为 .
(2)1.56g可以显+1价的某金属与足量盐酸完全反应,生成0.04g氢气,则该金属的摩尔质量为
考点:物质的量的相关计算
专题:计算题
分析:(1)根据n=
=
计算;
(2)金属为+1价,设金属为M,反应的方程式为2M+2HCl=2MCl+H2↑,结合方程式计算.
| V |
| Vm |
| m |
| M |
(2)金属为+1价,设金属为M,反应的方程式为2M+2HCl=2MCl+H2↑,结合方程式计算.
解答:
解:(1)n=
=0.005mol,
M=
=28g/mol,相对分子质量为28,
故答案为:28;
(2)n(H2)=
=0.02mol,
金属为+1价,设金属为M,反应的方程式为2M+2HCl=2MCl+H2↑,
由方程式可知,金属的物质的量为0.04mol,
则金属的摩尔质量为
=39g/mol,
故答案为:39g/mol.
| 0.112L |
| 22.4L/mol |
M=
| 0.14g |
| 0.005mol |
故答案为:28;
(2)n(H2)=
| 0.04g |
| 2g/mol |
金属为+1价,设金属为M,反应的方程式为2M+2HCl=2MCl+H2↑,
由方程式可知,金属的物质的量为0.04mol,
则金属的摩尔质量为
| 1.56g |
| 0.04mol |
故答案为:39g/mol.
点评:本题考查物质的量的相关计算,为高频考点,题目难度不大,本题注意相关物质的量的相关计算公式的运用,把握物质的量应用于化学方程式的计算.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
一氧化氮和一氧化碳都是汽车尾气里的有害物质,它们能缓慢地发生如下反应:2NO(g)+2CO(g)?N2(g)+2CO2(g)(正反应为放热反应).现利用此反应,拟设计一种环保装置以减轻汽车尾气对大气的污染.下列设计方案可以提高尾气处理效果的是( )
| A、不断向装置中鼓入空气 |
| B、提高反应装置的温度 |
| C、降低反应装置的压强 |
| D、在反应装置中装入碱石灰 |
下列说法正确的是( )
| A、用湿润的PH试纸可测溶液的酸碱性 |
| B、用碱式滴定管可量取5.00mLKMnO4溶液 |
| C、碳酸钠溶液可盛放于玻璃瓶塞的试剂瓶内 |
| D、氯水可用棕色试剂瓶保存于阴暗处 |
 我国已投入大量资金对饮用水设施进行全面改造,而合格的饮用水,离不开对水源进行澄清、过滤、消毒等处理.
我国已投入大量资金对饮用水设施进行全面改造,而合格的饮用水,离不开对水源进行澄清、过滤、消毒等处理.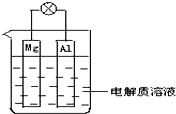 (1)如图所示,组成一种原电池.试回答下列问题(灯泡功率合适):
(1)如图所示,组成一种原电池.试回答下列问题(灯泡功率合适):