题目内容
下列化学反应中电子转移的表示方法不正确的是( )
A、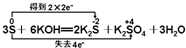 |
B、 |
C、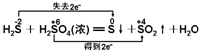 |
D、 |
考点:氧化还原反应的电子转移数目计算
专题:氧化还原反应专题
分析:氧化还原反应中失电子的元素化合价升高,得电子的元素化合价降低,化合价降低数目=化合价升高数目=转移的电子数目.
解答:
解:A.S元素化合价由0价升高为+4价,失去电子,S元素得到电子,化合价从0价降低为-2价,共降低4价,转移电子为4e-,故A正确;
B.Fe元素化合价由+3降低为0价,总共降低6价,得到6个电子,Al元素从0价升高为+3价,共失去6个电子,故B错误;
C.S元素化合价由-2价升高为0价,失去电子,S元素化合价从+6价降低为+4价,共降低2价,转移电子2e-,故C正确;
D.铁元素化合价由0价变为+3价,N元素化合价由+5价变为+4价,共转移电子数为3,故D正确;
故选B.
B.Fe元素化合价由+3降低为0价,总共降低6价,得到6个电子,Al元素从0价升高为+3价,共失去6个电子,故B错误;
C.S元素化合价由-2价升高为0价,失去电子,S元素化合价从+6价降低为+4价,共降低2价,转移电子2e-,故C正确;
D.铁元素化合价由0价变为+3价,N元素化合价由+5价变为+4价,共转移电子数为3,故D正确;
故选B.
点评:本题考查氧化还原反应的特征和实质知识,中等难度,关键判断准化合价变化总数.

练习册系列答案
相关题目
下列关于化学键的说法中不正确的是( )
| A、化学键是一种作用力 |
| B、非极性键不是化学键 |
| C、化学反应过程中,反应物内的化学键断裂,产物中的化学键形成 |
| D、化学键可以使离子相结合,也可以使原子相结合 |
若NA表示阿伏加德罗常数的值,在3(NH4)2SO4
N2+4NH3↑+3SO2↑+6H2O中,当有12NA个电子转移时,以下说法正确的是( )
| ||
| A、有6molS(+6价)被还原 |
| B、有4molSO2生成 |
| C、有4molN(-3价)被还原 |
| D、有8mol(NH4)2SO4分解 |
下列反应与Na2O2+SO2→Na2SO4相比较,Na2O2的作用相同的是( )
| A、2Na2O2+2CO2→2Na2CO3+O2 |
| B、2Na2O2+2SO3→2Na2SO4+O2 |
| C、Na2O2+H2SO4→Na2SO4+H2O2 |
| D、3Na2O2+Cr2O3→2Na2CrO4+Na2O |
根据有机化合物的命名原则,下列命名正确的是( )
A、 4-甲基-1,2-戊炔 4-甲基-1,2-戊炔 |
| B、CH3CH(CH3)CH=CHCH3 2-甲基-3-戊烯 |
C、 2,2,3-甲基戊烷 2,2,3-甲基戊烷 |
D、 间二硝基苯 间二硝基苯 |
如图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中.下列正确的是( )


| A、K1闭合,铁棒上发生的反应为2H++2e→H2↑ |
| B、K1闭合,石墨棒周围溶液pH逐渐升高 |
| C、K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法 |
| D、K2闭合,电路中通过0.002NA个电子时,两极共产生0.001mol气体 |
某物质分子式为 C2H4,下列说法不正确的是( )
| A、该分子中既含有极性共价键,又含有非极性共价键 |
| B、该分子是极性分子 |
| C、该分子中六个原子位于同一平面,键角为120° |
| D、该物质难溶于水 |
下列关于容量瓶及其使用方法的叙述,正确的是( )
| A、是配制一定物质的量浓度的溶液的专用仪器 |
| B、容量瓶可以用来加热 |
| C、不能用容量瓶贮存配制好的溶液 |
| D、可以用500mL容量瓶配制250mL溶液 |
下列说法正确的是( )
| A、PM2.5作为空气质量预报的一项重要指标,它是指空气中直径大于或等于2.5μm的颗粒物,该值越高,代表空气污染程度越严重 |
| B、新型材料聚酯纤维、光导纤维都属于有机高分子 |
| C、上海世博会很多展馆采用光电转化装置,体现当今“低碳”经济的理念 |
| D、塑化剂是一种化工塑料软化剂,可以大量添加到婴幼儿玩具中 |