题目内容
若NA表示阿伏加德罗常数的值,在3(NH4)2SO4
N2+4NH3↑+3SO2↑+6H2O中,当有12NA个电子转移时,以下说法正确的是( )
| ||
| A、有6molS(+6价)被还原 |
| B、有4molSO2生成 |
| C、有4molN(-3价)被还原 |
| D、有8mol(NH4)2SO4分解 |
考点:氧化还原反应的计算
专题:氧化还原反应专题
分析:(NH4)2SO4在强热分解的产物是SO2、N2、NH3和H2O,则N元素的化合价由-3价升高为0,S元素的化合价由+6价降低为+4,结合化合价的变化来解答.
解答:
解:A.反应中S元素化合价由+6价降低到+4价,被还原,则当有12NA个电子转移时,有6molS被还原,故A正确;
B.由方程式可知,转移12mol电子,有6mol SO2生成,故B错误;
C.反应中N元素化合价由-3价升高到0价,被氧化,故C错误;
D.由方程式可知,当有3mol (NH4)2SO4参加反应时,生成3mol SO2,转移6mol电子,则转移12mol电子,有6mol(NH4)2SO4分解,故D错误.
故选A.
B.由方程式可知,转移12mol电子,有6mol SO2生成,故B错误;
C.反应中N元素化合价由-3价升高到0价,被氧化,故C错误;
D.由方程式可知,当有3mol (NH4)2SO4参加反应时,生成3mol SO2,转移6mol电子,则转移12mol电子,有6mol(NH4)2SO4分解,故D错误.
故选A.
点评:本题考查氧化还原反应,为高考常见题型,把握反应中元素的化合价变化为解答的关键,由元素的化合价变化及电子守恒的角度解答该题,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
1.0mol?L-1的NaCl溶液表示( )
| A、溶液中含有1mol NaCl |
| B、1mol NaCl 溶于1L水中 |
| C、58.5g NaCl溶于941.5g水中 |
| D、1L溶液里含有NaCl 58.5g |
下列说法正确的是( )
| A、乙炔的结构简式为CHCH |
| B、羟基(一OH)和氢氧根(OH一)的电子数不同 |
C、对甲基苯甲醛的结构简式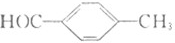 |
D、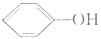 与 与 互为同系物 互为同系物 |
在100mL 0.1mol/L NaOH溶液中,所含NaOH的质量是( )
| A、40g | B、4g |
| C、0.4g | D、0.04g |
制取下列气体,不宜采取排空气法收集的是( )
| A、氨气 | B、乙烯 |
| C、二氧化碳 | D、二氧化氮 |
如图是模拟“侯氏制减法”制取NaHCO3的部分装置.下列操作正确的是( )


| A、a通入C02,然后b通入NH3,c中放碱石灰 |
| B、b通入NH3,然后a通入CO2,c中放碱石灰 |
| C、a通入NH3,然后b通入CO2,c中放蘸稀硫酸的脱脂棉 |
| D、b通入C02,然后a通入NH3,c中放蘸稀硫酸的脱脂棉 |
根据我校艺体中心吴主任要求,工作人员要定期对游泳池进行消毒.下列物质适用于泳池消毒的是( )
| A、烧碱 | B、盐酸 |
| C、活性炭 | D、漂白粉 |
下列化学反应中电子转移的表示方法不正确的是( )
A、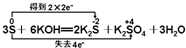 |
B、 |
C、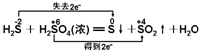 |
D、 |
下列有关氢化物的叙述中正确的是( )
| A、稳定性:H2S>HF |
B、HCl的电子式为  |
| C、一个D216O分子所含的中子数为8 |
| D、在卤化氢中HF最稳定 |