题目内容
下列反应与Na2O2+SO2→Na2SO4相比较,Na2O2的作用相同的是( )
| A、2Na2O2+2CO2→2Na2CO3+O2 |
| B、2Na2O2+2SO3→2Na2SO4+O2 |
| C、Na2O2+H2SO4→Na2SO4+H2O2 |
| D、3Na2O2+Cr2O3→2Na2CrO4+Na2O |
考点:真题集萃,钠的重要化合物
专题:元素及其化合物
分析:因为在Na2O2+SO2→Na2SO4中,Na2O2的作用相同的是氧化剂,所以,
A、在2Na2O2+2CO2→2Na2CO3+O2中Na2O2是自身氧化还原;
B、在2Na2O2+2SO3→2Na2SO4+O2中Na2O2是自身氧化还原;
C、在Na2O2+H2SO4→Na2SO4+H2O2中这是非氧化还原,是一个复分解反应;
D、在3Na2O2+Cr2O3→2Na2CrO4+Na2O中,Na2O2中-1价的氧变为-2价,Na2O2作还原剂,据此作判断.
A、在2Na2O2+2CO2→2Na2CO3+O2中Na2O2是自身氧化还原;
B、在2Na2O2+2SO3→2Na2SO4+O2中Na2O2是自身氧化还原;
C、在Na2O2+H2SO4→Na2SO4+H2O2中这是非氧化还原,是一个复分解反应;
D、在3Na2O2+Cr2O3→2Na2CrO4+Na2O中,Na2O2中-1价的氧变为-2价,Na2O2作还原剂,据此作判断.
解答:
解:因为在Na2O2+SO2→Na2SO4中,Na2O2的作用相同的是氧化剂,所以,
A、在2Na2O2+2CO2→2Na2CO3+O2中Na2O2是自身氧化还原,故A错误;
B、在2Na2O2+2SO3→2Na2SO4+O2中Na2O2是自身氧化还原,故B错误;
C、在Na2O2+H2SO4→Na2SO4+H2O2中这是非氧化还原,是一个复分解反应,故C错误;
D、在3Na2O2+Cr2O3→2Na2CrO4+Na2O中,Na2O2中-1价的氧变为-2价,Na2O2作氧化剂,故D正确;
故选D.
A、在2Na2O2+2CO2→2Na2CO3+O2中Na2O2是自身氧化还原,故A错误;
B、在2Na2O2+2SO3→2Na2SO4+O2中Na2O2是自身氧化还原,故B错误;
C、在Na2O2+H2SO4→Na2SO4+H2O2中这是非氧化还原,是一个复分解反应,故C错误;
D、在3Na2O2+Cr2O3→2Na2CrO4+Na2O中,Na2O2中-1价的氧变为-2价,Na2O2作氧化剂,故D正确;
故选D.
点评:本题主要考查了学生对氧化还原反应的理解,解题的关键是抓住化合价的变化分析,中等难度.

练习册系列答案
相关题目
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
| A、电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-→Cl2↑ |
| B、氢氧燃料电池的负极反应式:O2+2H2O+4e-→4OH- |
| C、粗铜精炼时,与电源正极相连的是粗铜,电极反应式为:Cu-2e-→Cu2+ |
| D、钢铁发生电化腐蚀的正极反应式:Fe-2e-→Fe2+ |
在100mL 0.1mol/L NaOH溶液中,所含NaOH的质量是( )
| A、40g | B、4g |
| C、0.4g | D、0.04g |
如图是模拟“侯氏制减法”制取NaHCO3的部分装置.下列操作正确的是( )


| A、a通入C02,然后b通入NH3,c中放碱石灰 |
| B、b通入NH3,然后a通入CO2,c中放碱石灰 |
| C、a通入NH3,然后b通入CO2,c中放蘸稀硫酸的脱脂棉 |
| D、b通入C02,然后a通入NH3,c中放蘸稀硫酸的脱脂棉 |
根据我校艺体中心吴主任要求,工作人员要定期对游泳池进行消毒.下列物质适用于泳池消毒的是( )
| A、烧碱 | B、盐酸 |
| C、活性炭 | D、漂白粉 |
下列叙述中正确的是( )
(1)纯铁比碳素钢易生锈(2)用氨水除去试管上的银镜
(3)硅是制作光导纤维和制造太阳能电池的主要原料
(4)可用稀盐酸、碳酸钠溶液、硅酸钠溶液设计实验来验证元素的非金属性Cl>C(碳)>Si
(5)催化剂只能改变反应的活化能,不能改变反应的热效应
(6)用氢氟酸雕刻玻璃是利用氢氟酸能与二氧化硅反应的性质
(7)同主族元素的简单阴离子还原性越强,水解程度越大
(8)Al2O3在工业上用于制作耐高温材料,也用于电解法治炼铝
(9)丁达尔效应可用于区别溶液与胶体,云、雾均能产生丁达尔效应
(10)明矾可用于水的消毒、杀菌;碳酸钡可用于钡餐透视
(11)用浸泡过的高锰酸钾溶液的硅藻土吸收水果释放的乙烯,可达到水果保鲜的目的
(12)同周期金属元素的化合价越高,其原子失电子能力越弱.
(1)纯铁比碳素钢易生锈(2)用氨水除去试管上的银镜
(3)硅是制作光导纤维和制造太阳能电池的主要原料
(4)可用稀盐酸、碳酸钠溶液、硅酸钠溶液设计实验来验证元素的非金属性Cl>C(碳)>Si
(5)催化剂只能改变反应的活化能,不能改变反应的热效应
(6)用氢氟酸雕刻玻璃是利用氢氟酸能与二氧化硅反应的性质
(7)同主族元素的简单阴离子还原性越强,水解程度越大
(8)Al2O3在工业上用于制作耐高温材料,也用于电解法治炼铝
(9)丁达尔效应可用于区别溶液与胶体,云、雾均能产生丁达尔效应
(10)明矾可用于水的消毒、杀菌;碳酸钡可用于钡餐透视
(11)用浸泡过的高锰酸钾溶液的硅藻土吸收水果释放的乙烯,可达到水果保鲜的目的
(12)同周期金属元素的化合价越高,其原子失电子能力越弱.
| A、(1)(4)(5)(6)(7)(11)(12) |
| B、(2)(3)(5)(7)(9)(12) |
| C、(1)(3)(4)(5)(6)(11) |
| D、(5)(6)(8)(9)(11)(12) |
下列化学反应中电子转移的表示方法不正确的是( )
A、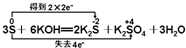 |
B、 |
C、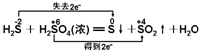 |
D、 |
向盛有乙醇的烧杯中投入一小块金属钠,不能看到的现象是( )
| A、钠表面产生气泡 |
| B、钠沉在乙醇液面以下 |
| C、钠块熔成小球 |
| D、钠在反应的过程中上升 |
短周期元素X、Y、Z和W的原子序数依次增大.X原子的S能级电子总数是P能级电子总数的2倍,Y与X同主族,Z和W原子中未成对电子数之比为2:1.下列说法错误的是( )
| A、XW4为非极性分子 |
| B、Y、Z、W的最高价氧化物的水化物酸性强弱顺序是Y<Z<W |
| C、X、Y的氢化物由固态转化为气态时,克服相同的作用力 |
| D、XW4、YW4、ZW2分子中的中心原子均为sp杂化 |