题目内容
下列关于化学键的说法中不正确的是( )
| A、化学键是一种作用力 |
| B、非极性键不是化学键 |
| C、化学反应过程中,反应物内的化学键断裂,产物中的化学键形成 |
| D、化学键可以使离子相结合,也可以使原子相结合 |
考点:化学键
专题:化学键与晶体结构
分析:化学键是相邻原子之间强烈的相互作用,离子键和共价键均为化学键,化学反应的实质为旧键断裂、新键形成,以此来解答.
解答:
解:A.化学键是相邻原子之间强烈的相互作用,则化学键是一种作用力,故A正确;
B.非极性键为共价键,属于化学键,故B错误;
C.由化学反应的实质可知,化学反应过程中,反应物内的化学键断裂,产物中的化学键形成,故C正确;
D.离子键和共价键均为化学键,则化学键可以使离子相结合,也可以使原子相结合,故D正确;
故选B.
B.非极性键为共价键,属于化学键,故B错误;
C.由化学反应的实质可知,化学反应过程中,反应物内的化学键断裂,产物中的化学键形成,故C正确;
D.离子键和共价键均为化学键,则化学键可以使离子相结合,也可以使原子相结合,故D正确;
故选B.
点评:本题考查化学键,为高频考点,把握化学键的概念、分类及化学反应的实质为解答的关键,侧重基础知识的考查,题目难度不大.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
下列各组中两种元素金属性或非金属性的强弱比较正确是( )
| A、金属性:Na大于K |
| B、金属性:B大于Al |
| C、非金属性:P小于Cl |
| D、非金属性:S大于Cl |
1.0mol?L-1的NaCl溶液表示( )
| A、溶液中含有1mol NaCl |
| B、1mol NaCl 溶于1L水中 |
| C、58.5g NaCl溶于941.5g水中 |
| D、1L溶液里含有NaCl 58.5g |
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
| A、电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-→Cl2↑ |
| B、氢氧燃料电池的负极反应式:O2+2H2O+4e-→4OH- |
| C、粗铜精炼时,与电源正极相连的是粗铜,电极反应式为:Cu-2e-→Cu2+ |
| D、钢铁发生电化腐蚀的正极反应式:Fe-2e-→Fe2+ |
在化学反应中,原子内会发生变化的是( )
| A、质子数 | B、中子数 |
| C、核外电子数 | D、质量数 |
20℃时,饱和KCl溶液的密度为1.174g/cm3,物质的量浓度为4.0mol/L,则下列说法中,正确的是( )
| A、20℃时,密度小于1.174 g/cm3的KCl溶液也可能是饱和溶液 | ||
B、此溶液中KCl的质量分数为
| ||
| C、25℃时,饱和KCl溶液的浓度大于4.0 mol/L | ||
| D、将此溶液蒸发部分水,再恢复到20℃时,溶液密度一定大于1.174 g/cm3 |
下列说法正确的是( )
| A、乙炔的结构简式为CHCH |
| B、羟基(一OH)和氢氧根(OH一)的电子数不同 |
C、对甲基苯甲醛的结构简式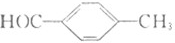 |
D、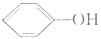 与 与 互为同系物 互为同系物 |
在100mL 0.1mol/L NaOH溶液中,所含NaOH的质量是( )
| A、40g | B、4g |
| C、0.4g | D、0.04g |
下列化学反应中电子转移的表示方法不正确的是( )
A、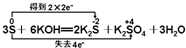 |
B、 |
C、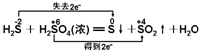 |
D、 |