题目内容
1.1.204×1024个硫原子中有2mol硫原子,有32NA个质子.分析 结合n=$\frac{N}{{N}_{A}}$及分子构成计算.
解答 解:1.204×1024个硫原子中有$\frac{1.204×1{0}^{24}}{6.02×1{0}^{23}}$=2mol硫原子,有2mol×16×NA=32NA个质子,
故答案为:2;32NA.
点评 本题考查物质的量的计算,为高频考点,把握物质的量、微粒数的关系为解答的关键,侧重分析与计算能力的考查,注意基本计算公式的应用,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
11.下列离子方程式改写成化学方程式正确的是( )
| A. | Cu2++2OH-=Cu(OH)2↓CuCO3+2NaOH═Cu(OH)2↓+Na2CO3 | |
| B. | CO32-+2H+=CO2↑+H2OBaCO3+2HCl═BaCl2+CO2↑+H2O | |
| C. | Ca2++CO32-=CaCO3↓Ca(NO3)2+Na2CO3═CaCO3↓+NaNO3 | |
| D. | H++OH-=H2OBa(OH)2+H2SO4═BaSO4↓+2H2O |
12.以NA代表阿伏加德罗常数的值,则关于热化学方程式C2H2(g)+$\frac{5}{2}$O2(g)→2CO2(g)+H2O(l)△H=-1300kJ•mol-1的说法中,正确的是( )
| A. | 当10NA个电子转移时,该反应放出1300 kJ的能量 | |
| B. | 当1NA个水分子生成且为液体时,吸收1300 kJ的能量 | |
| C. | 当2NA个碳氧共用电子对生成时,放出1300 kJ的能量 | |
| D. | 当8NA个碳氧共用电子对生成时,吸收1300 kJ的能量 |
9.下列说法中,正确的是( )
| A. | 22.4 L氧气中,一定含有2 mol氧原子 | |
| B. | 80 g NaOH溶解在1 L水中,得到溶液的物质的量浓度为2mol/L | |
| C. | 18 g水在标准状况下的体积约为22.4 L | |
| D. | 标准状况下,20 mL NH3跟60 mL O2所含分子个数比为1:3 |
16.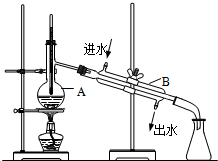 如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题.
如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题.
(1)图中有两处明显的错误是
①水银球未在蒸馏烧瓶的支管口处;
②冷却水未下进上出.
(2)A仪器的名称是圆底烧瓶,B仪器的名称是直形冷凝管.
 如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题.
如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题.(1)图中有两处明显的错误是
①水银球未在蒸馏烧瓶的支管口处;
②冷却水未下进上出.
(2)A仪器的名称是圆底烧瓶,B仪器的名称是直形冷凝管.
13.当氢氧化钙固体在水中达到溶解平衡时,为使Ca(OH)2固体的量减少,需加入少量的( )
| A. | NH4NO3固体 | B. | NaOH固体 | C. | CaCl2固体 | D. | NaHSO4固体 |
 .
. .
. 元素A、B、C、D、E、F是位于元素周期表前四周期元素,且原子序数依次增大.其中 D、F为常见金属元素;A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标准状况下的密度为0.759g•L-1,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族,由D或F元素组成的单质或某些离子(或化合物)在溶液中均有下列转化关系(如图,其它参与反应的物质未列出):
元素A、B、C、D、E、F是位于元素周期表前四周期元素,且原子序数依次增大.其中 D、F为常见金属元素;A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标准状况下的密度为0.759g•L-1,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族,由D或F元素组成的单质或某些离子(或化合物)在溶液中均有下列转化关系(如图,其它参与反应的物质未列出):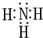 .
.