题目内容
有机物A是农药生产中的一种中间体,结构简式如图所示.下列叙述中正确的是( )


| A、1 mol A最多能与4 mol H2发生加成反应 |
| B、有机物A可以在一定条件下与HBr发生反应 |
| C、有机物A与浓硫酸混合加热,可以发生消去反应 |
| D、1 mol A与足量的NaOH溶液反应,最多可以消耗 2 mol NaOH |
考点:有机物的结构和性质
专题:
分析:由结构简式可知,分子中含苯环、-COOC-、-OH、-Cl,结合苯、酯、醇、卤代烃的性质来解答.
解答:
解:A.只有苯环与氢气发生加成反应,则1 mol A最多能与3 mol H2发生加成反应,故A错误;
B.含-OH,则有机物A可以在一定条件下与HBr发生取代反应,故B正确;
C.与-OH相连C的邻位C上没有H,则与浓硫酸混合加热,不能发生消去反应,故C错误;
D.-COOC-、-OH及-COOC-水解生成的酚-OH均与NaOH反应,则1 mol A与足量的NaOH溶液反应,最多可以消耗3 mol NaOH,故D错误;
故选B.
B.含-OH,则有机物A可以在一定条件下与HBr发生取代反应,故B正确;
C.与-OH相连C的邻位C上没有H,则与浓硫酸混合加热,不能发生消去反应,故C错误;
D.-COOC-、-OH及-COOC-水解生成的酚-OH均与NaOH反应,则1 mol A与足量的NaOH溶液反应,最多可以消耗3 mol NaOH,故D错误;
故选B.
点评:本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重苯、酯、醇、卤代烃及分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、含有NA个氦原子的氦气在标准状况下的体积约为11.2 L |
| B、在常温常压下,11.2 L Cl2含有的分子数约为0.5 NA |
| C、25℃,1.01×105Pa,64 g SO2中含有的原子数为3 NA |
| D、标准状况下,11.2 L H2O含有的分子数为0.5 NA |
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )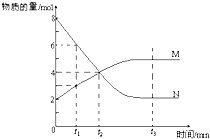

| A、反应的化学方程式为:N?2M |
| B、t2时,正逆反应速率相等,达到平衡 |
| C、t3时,正反应速率大于逆反应速率 |
| D、t1时,N的浓度是M浓度的2倍 |
下列物质转化关系中,必须加入适当氧化剂才能实现的是( )
| A、PCl3→PCl5 |
| B、MnO4-→Mn2+ |
| C、SO3→SO42- |
| D、CO2→CO |
下列有关说法正确的是( )
| A、若在海轮外壳上附着一些铜块,则可以减缓海轮外壳的腐蚀 |
| B、2NO(g)+2CO(g)=N2(g)+2CO2(g)在常温下能自发进行,则该反应的△H<0 |
| C、增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应能增大生成H2的速率 |
| D、对于乙酸与乙醇的酯化反应(△H<0),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大 |