题目内容
8.下列是四种烷烃分子的结构模型图,其中沸点最高的是( )| A. |  | B. | 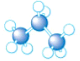 | C. | 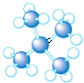 | D. | 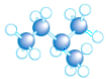 |
分析 这几种物质都是烷烃,且都是分子晶体,烷烃中碳原子个数越多其熔沸点越高,同分异构体中支链越多其熔沸点越低,据此分析解答.
解答 解:这几种物质都是烷烃,且都是分子晶体,烷烃中碳原子个数越多其熔沸点越高,同分异构体中支链越多其熔沸点越低,C、D属于同分异构体,C中支链大于D,所以熔沸点高低顺序是D>C>B>A,则熔沸点最高的是正戊烷,故选D.
点评 本题考查晶体熔沸点高低判断,明确分子晶体熔沸点与相对分子质量、氢键、烃中支链等之间的关系即可解答,题目难度不大.

练习册系列答案
相关题目
18.生命起源于海洋,科学家认为,由于海洋中Al3+的浓度极低,所以Al元素未成为人体内的必需元素,相反它对人体有害,下列有关铝的说法中不正确的是( )
| A. | 家庭不宜用铝锅长期盛放菜,汤等食品 | |
| B. | 明矾[KAl(SO4)2•12H2O]含结晶水,是混合物 | |
| C. | Al既能与盐酸反应,又能与NaOH溶液反应 | |
| D. | 铝热反应是放热反应 |
19.某溶液中有Mg2+、Fe2+、Cu2+三种离子,向其中加入过量的NaOH溶液后过滤,将滤渣高温灼烧并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是( )
| A. | Mg2+ | B. | Fe2+ | C. | Cu2+ | D. | 无减少 |
3.2008年北京奥运会的“祥云”火炬所用燃料的主要成分是丙烷,下列有关丙烷的叙述中,不正确的是( )
| A. | 分子中碳原子不在一条直线上 | B. | 光照不能够发生取代反应 | ||
| C. | 是石油分馏的一种产品 | D. | 比丁烷更易液化 |
13.几种短周期元素的原子半径及某些化合价见下表:
分析上表中有关数据,并结合已学过的知识,回答以下问题.涉及上述元素的答案,请用元素符号表示.
(1)E元素在周期表中位于三周期ⅥA族;
(2)A、H、J对应的离子半径由大到小的顺序是(填写离子符号)F-、Na+、Al3+
(3)J单质在B单质中燃烧可生成化合物X,X的电子式是 ,其中所含的化学键类型为离子键和非极性键.
,其中所含的化学键类型为离子键和非极性键.
(4)I单质可在D的最高价氧化物中燃烧,涉及的化学方程式为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MaO+C.
(5)B与H所形成的化合物与J的最高价氧化物对应水化物Y的溶液发生反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O.
| 元素代号 | A | B | D | E | G | H | I | J |
| 化合价 | -1 | -2 | +4、-4 | +4、-2 | +5、-3 | +3 | +2 | +1 |
| 原子半径/nm | 0.071 | 0.074 | 0.077 | 0.102 | 0.110 | 0.143 | 0.160 | 0.186 |
(1)E元素在周期表中位于三周期ⅥA族;
(2)A、H、J对应的离子半径由大到小的顺序是(填写离子符号)F-、Na+、Al3+
(3)J单质在B单质中燃烧可生成化合物X,X的电子式是
 ,其中所含的化学键类型为离子键和非极性键.
,其中所含的化学键类型为离子键和非极性键.(4)I单质可在D的最高价氧化物中燃烧,涉及的化学方程式为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MaO+C.
(5)B与H所形成的化合物与J的最高价氧化物对应水化物Y的溶液发生反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O.