题目内容
16.根据新制氯水的成分填空(填化学式):(1)使氯水呈黄绿色的是Cl2;
(2)能使AgNO3溶液产生白色沉淀的是HCl;
(3)能使无水硫酸铜显蓝色的是H2O;
(4)能使红色布条褪色的是HClO;
(5)能与NaHCO3溶液反应放出气体的是HCl.
分析 氯气溶于水发生反应Cl2+H2O?HCl+HClO,新制氯水含有Cl2、H2O、HClO、H+、Cl-等粒子,其中H+可与碳酸钙等物质反应,而Cl2、HClO具有强氧化性,HClO具有漂白性,溶液中含有Cl-可与硝酸银反应生成白色AgCl沉淀,以此解答该题.
解答 解:(1)使氯水呈黄绿色的是氯气;
(2)能使AgNO3溶液产生白色沉淀的是盐酸电离产生的氯离子;
(3)能使无水硫酸铜显蓝色的是水,生成硫酸铜晶体;
(4)能使红色布条褪色的是次氯酸的氧化性漂白;
(5)能与NaHCO3溶液反应放出气体的是盐酸电离产生的氢离子;
故答案为:(1)Cl2;(2)HCl;(3)H2O;(4)HClO;(5)HCl.
点评 本题综合考查氯气和氯水的性质,注意把握氯气和水反应的特点以及氯水的成分和性质,为高考高频考点,侧重于基础知识的综合运用,难度不大.

练习册系列答案
相关题目
6.下列溶液中微粒的物质的量浓度关系正确的是( )
| A. | 0.1 mol•L-1某二元弱酸的酸式盐NaHA溶液中:c(Na+)=2c(A2-)+c(HA-)+c(H2A) | |
| B. | 某酸式盐NaHY的水溶液显碱性,该酸式盐溶液中离子浓度关系为:c(Na+)>c(HY-)>c(OH-)>c(H+) | |
| C. | 物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+c(OH-)=c(H+)+c(CH3COOH) | |
| D. | 25℃,pH=12的氨水和pH=2的盐酸等体积混合:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
7.柴静的调查报告《苍穹之下》引起人们对雾霾的更大关注.某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5微米的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
(1)将PM2.5样本用蒸馏水处理制成待测试样,测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断试样的pH=4.
(2)洗涤含SO2的烟气,下列物质可作洗涤剂的是bc
a.CaCl2 溶液 b.Na2CO3 溶液 c.Ca(OH)2 悬浊液 d.浓H2SO4
(3)安装汽车尾气催化转化器也可减轻PM2.5的危害,其反应是:
2NO(g)+2CO(g)$\frac{\underline{\;催化剂\;}}{\;}$2CO2(g)+N2(g);△H<0
①该反应平衡常数表达式K=$\frac{{c}^{2}(C{O}_{2})c({N}_{2})}{{c}^{2}(NO){c}^{2}(CO)}$;温度升高K值减小(填“增大”或“减小”)
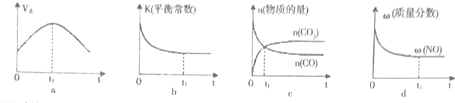
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是bd.
(4)汽车尾气中NOx和CO的生成及转化.
①已知汽缸中生成NO的反应为N2(g)+O2(g)?2NO(g)△H>0,汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是温度升高,平衡正向移动,NO的含量增大.
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)═2C(s)+O2(g)△H>0,判断该设想能否实现:不能(填“能”或“不能”),简述其依据:;△H>0△S<0,则在任何温度下△G>0,不可能自发进行.
(1)将PM2.5样本用蒸馏水处理制成待测试样,测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离 子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
(2)洗涤含SO2的烟气,下列物质可作洗涤剂的是bc
a.CaCl2 溶液 b.Na2CO3 溶液 c.Ca(OH)2 悬浊液 d.浓H2SO4
(3)安装汽车尾气催化转化器也可减轻PM2.5的危害,其反应是:
2NO(g)+2CO(g)$\frac{\underline{\;催化剂\;}}{\;}$2CO2(g)+N2(g);△H<0
①该反应平衡常数表达式K=$\frac{{c}^{2}(C{O}_{2})c({N}_{2})}{{c}^{2}(NO){c}^{2}(CO)}$;温度升高K值减小(填“增大”或“减小”)
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是bd.

(4)汽车尾气中NOx和CO的生成及转化.
①已知汽缸中生成NO的反应为N2(g)+O2(g)?2NO(g)△H>0,汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是温度升高,平衡正向移动,NO的含量增大.
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)═2C(s)+O2(g)△H>0,判断该设想能否实现:不能(填“能”或“不能”),简述其依据:;△H>0△S<0,则在任何温度下△G>0,不可能自发进行.
4.下列反应中水作为氧化剂的是( )
| A. | Cl2+H2O═HCl+HClO | B. | 3Fe+4H2O(g)$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2 | ||
| C. | 2F2+2H2O═4HF+O2 | D. | 3NO2+H2O═2HNO3+NO |
11.下列与有机物的结构、性质有关的叙述正确的是( )
| A. | 苯、苯的同系物均不能使酸性KMnO4溶液褪色 | |
| B. | 甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应 | |
| C. | 芳香烃可以来自于煤干馏产品中的煤焦油 | |
| D. | 乙醇、乙酸均能与Na反应放出H2,二者分子中官能团相同 |
1.下列物质中,属于酚类的是 ( )
| A. | 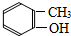 | B. | 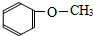 | C. | 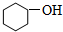 | D. | 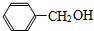 |
8.下列是四种烷烃分子的结构模型图,其中沸点最高的是( )
| A. |  | B. | 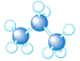 | C. | 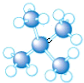 | D. | 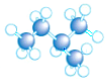 |
5.从防火、灭火、自救等安全知识判断,下列做法正确的是( )
| A. | 室内着火马上开门窗 | B. | 炒菜时油锅着火用锅盖盖灭 | ||
| C. | 用明火检验燃气是否泄漏 | D. | 电器着火时用水浇灭 |
13. X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )
 X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )| A. | 最高价氧化物对应水化物的酸性W比Z弱 | |
| B. | 只由这四种元素不能组成有机化合物 | |
| C. | Z的单质与氢气反应较Y剧烈 | |
| D. | X、Y形成的化合物都易溶于水 |