题目内容
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、1 mol-CH3和1 mol OH-都含有10 NA个电子 |
| B、常温常压下,8gCH4含有2NA个共价键 |
| C、1L 0.1 mol?L-1的醋酸溶液中含有0.1NA个H+ |
| D、标准状况下22.4 L 乙醇含碳原子数为NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、一个-CH3中含有9个电子,一个OH-中含有10个电子,根据N=nNA计算;
B、甲烷( )分子中含有4个碳氢共价键;
)分子中含有4个碳氢共价键;
C、醋酸是弱电解质,不能完全电离;
D、标况下,乙醇为液态.
B、甲烷(
 )分子中含有4个碳氢共价键;
)分子中含有4个碳氢共价键;C、醋酸是弱电解质,不能完全电离;
D、标况下,乙醇为液态.
解答:
解:A、一个-CH3中含有9个电子,一个OH-中含有10个电子,所以1mol-CH3含有9NA个电子,1molOH-含有10NA个电子,故A错误;
B、8g甲烷的物质的量为0.5mol,甲烷的电子式为: ,0.5mol甲烷中含有2mol碳氢键,含有的共价键数约为2NA,故B正确;
,0.5mol甲烷中含有2mol碳氢键,含有的共价键数约为2NA,故B正确;
C、醋酸是弱电解质,不能完全电离,故溶液中的H+个数小于0.1NA个,故C错误;
D、标况下,乙醇为液态,故D错误.
故选B.
B、8g甲烷的物质的量为0.5mol,甲烷的电子式为:
 ,0.5mol甲烷中含有2mol碳氢键,含有的共价键数约为2NA,故B正确;
,0.5mol甲烷中含有2mol碳氢键,含有的共价键数约为2NA,故B正确;C、醋酸是弱电解质,不能完全电离,故溶液中的H+个数小于0.1NA个,故C错误;
D、标况下,乙醇为液态,故D错误.
故选B.
点评:本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构、状态是解题关键,难度不大.

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
下列说法不正确的是( )
| A、使用太阳能热水器、沼气的利用、玉米制乙醇都涉及到生物质能的利用 |
| B、石油、煤、天然气、可燃冰、植物油都属于化石燃料 |
| C、向汽油中添加甲醇后,该混合燃料的热值不变 |
| D、利用太阳能在催化剂参与下分解水制氢是把光能转化为化学能的绿色化学方法 |
NA代表阿伏加德罗常数,下列叙述错误的是( )
| A、10mL质量分数为98%的H2SO4,用水稀释至100mL,H2SO4的质量分数大于9.8% |
| B、在H2O2+Cl2=2HCl+O2反应中,每生成32g氧气,则转移电子个数为2moL |
| C、标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g |
| D、某无色溶液中通入Cl2,溶液变为棕黄色,再加入淀粉溶液,溶液变为蓝色,说明原溶液中存在I- |
设NA为阿伏加德罗常数,下列说法中正确的是( )
| A、1g氢气中所含有的分子数为NA |
| B、0.5mol/L的AlCl3溶液中含有氯离子数为1.5NA |
| C、27g铝与足量NaOH反应消耗OH-的数目为4NA |
| D、7.8g的Na2O2与水完全反应转移的电子数目为0.1NA |
下列说法正确的是( )
| A、1molCH4与Cl2发生取代反应最多消耗2molCl2 | ||
| B、乙酸乙酯的水解属于取代反应 | ||
C、CH3-CH═CH2+Cl2
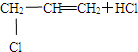 属于加成反应 属于加成反应 | ||
D、甲苯硝化生成三硝基甲苯的化学方程式 |
下列说法正确的是( )
| A、水加热到很高的温度都难分解是因为水分子中存在氢键 |
| B、蔗糖、淀粉、蛋白质及其水解产物均为非电解质 |
| C、在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH |
| D、不用任何试剂即可鉴别Na2CO3溶液和NaHSO4溶液. |
