题目内容
下列解释实验现象的反应方程式正确的是( )
| A、向Na2CO3溶液中滴入酚酞试液,溶液变红CO32-+2H2O?H2CO3+2OH- |
| B、向AgC1悬浊液中滴加Na2S溶液,白色沉淀变成黑色2AgC1+S2-=Ag2S↓+2C1- |
| C、铜器在潮湿的环境中表面生成一层“铜绿”:Cu+O2+CO2=CuCO3 |
| D、向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A、Na2CO3为二元弱酸正盐,分步水解,水解方程式也分布书写;
B、AgCl的溶解度大于Ag2S溶解度,所以AgCl的悬浊液中加入Na2S溶液可以转化为Ag2S;
C、铜器在潮湿的环境中表面生成一层“铜绿”是Cu2(OH)2CO3;
D、向NaHCO3溶液中加入过量的澄清石灰水,不可能存在CO32-.
B、AgCl的溶解度大于Ag2S溶解度,所以AgCl的悬浊液中加入Na2S溶液可以转化为Ag2S;
C、铜器在潮湿的环境中表面生成一层“铜绿”是Cu2(OH)2CO3;
D、向NaHCO3溶液中加入过量的澄清石灰水,不可能存在CO32-.
解答:
解:A、Na2CO3为二元弱酸正盐,分步水解,水解方程式也分布书写,CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-,故A错误;
B、AgCl的溶解度大于Ag2S溶解度,所以AgCl的悬浊液中加入Na2S溶液可以转化为Ag2S,离子方程式为:2AgC1+S2-=Ag2S↓+2C1-,故B正确;
C、铜器在潮湿的环境中表面生成一层“铜绿”是Cu2(OH)2CO3,2Cu+O2+H2O+CO2=Cu2(OH)2CO3,故C错误;
D、向NaHCO3溶液中加入过量的澄清石灰水,不可能存在CO32-,反应的离子方程式HCO3-+Ca2++OH-=CaCO3↓+H2O,故D错误;
故选B.
B、AgCl的溶解度大于Ag2S溶解度,所以AgCl的悬浊液中加入Na2S溶液可以转化为Ag2S,离子方程式为:2AgC1+S2-=Ag2S↓+2C1-,故B正确;
C、铜器在潮湿的环境中表面生成一层“铜绿”是Cu2(OH)2CO3,2Cu+O2+H2O+CO2=Cu2(OH)2CO3,故C错误;
D、向NaHCO3溶液中加入过量的澄清石灰水,不可能存在CO32-,反应的离子方程式HCO3-+Ca2++OH-=CaCO3↓+H2O,故D错误;
故选B.
点评:本题考查了盐类水解,沉淀溶解平衡的理解应用,酸式盐和碱反应量少的全部反应,掌握基础是关键,题目难度中等.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
用NA表示阿伏加德罗常数,下列说法正确的是( )
| A、78 g Na2O2与足量水反应中电子转移了0.2NA |
| B、1 mol甲基中含有7 NA 个电子 |
| C、62 g白磷中含P-P键为3 NA |
| D、1 mol氖气含有的原子数为2 NA |
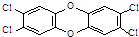 1999年比利时发生奶粉受二噁英污染事件.二噁英是一类芳香族化合物的多氯代衍生物的总称,结构稳定,难以被自然分解,是公认的最危险的致癌物质之一,2,3,7,8-四氯二苯并二噁英是其中的一种,结构如图.下列说法中不正确的是
1999年比利时发生奶粉受二噁英污染事件.二噁英是一类芳香族化合物的多氯代衍生物的总称,结构稳定,难以被自然分解,是公认的最危险的致癌物质之一,2,3,7,8-四氯二苯并二噁英是其中的一种,结构如图.下列说法中不正确的是( )
| A、它的分子式为C12H4O2Cl4 |
| B、它不能发生加成反应 |
| C、它的一溴取代物有一种 |
| D、此分子中共平面的原子最多有22个 |
化学与生活息息相关,下列说法正确的是( )
| A、HClO是弱酸,所以NaClO是弱电解质 |
| B、95℃纯水的pH<7,说明加热可导致水呈酸性 |
| C、放在冰箱中的食品保质期较长,这与温度对反应速率的影响有关 |
| D、自来水水阀生锈主要是化学腐蚀所致 |
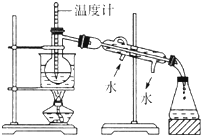 某化学课外小组以海带为原料制取少量碘水,现用CCl4 从碘水中萃取碘并用分液漏斗分离两种溶液.其实验可分解为如下各步:
某化学课外小组以海带为原料制取少量碘水,现用CCl4 从碘水中萃取碘并用分液漏斗分离两种溶液.其实验可分解为如下各步:


