题目内容
8.12mL浓度为0.1mol•L-1Na2SO3溶液,恰好与40mL浓度为0.01mol•L-1K2Cr2O7溶液完全反应,则元素Cr在被还原的产物中得化合价是( )| A. | 0 | B. | +2 | C. | +3 | D. | +6 |
分析 Na2SO3被氧化为Na2SO4,S元素化合价由+4价升高为+6价,K2Cr2O7中Cr元素发生还原反应,令Cr元素在产物中的化合价为a价,根据电子转移守恒计算a的值.
解答 解:令Cr元素在产物中的化合价为a价,根据电子转移守恒,则:
12×10-3L×0.1mol/L×(6-4)=40×10-3L×0.01mol/L×2×(6-a),
解得a=+3,
故选C.
点评 本题考查氧化还原反应计算、氧化还原反应概念等,难度中等,表示出得失数目是解题关键,熟练掌握电子转移守恒思想的运用.

练习册系列答案
相关题目
18.下列各组中互为同系物的是( )
| A. | 甲烷和丙烷 | B. |  和 和 | C. | 2-丙醇和1-丙醇 | D. | 2-丁烯和丙烯 |
19.下列物质的俗名与化学式不对应的是( )
| A. | 硅石--SiO2 | B. | 硫铁矿--FeS2 | ||
| C. | 纯碱--NaOH | D. | 芒硝--Na2SO4•10H2O |
16.化学与生活密切相关,下列有关说法错误的是( )
| A. | 食醋可用于除去水垢,食醋的主要成分乙酸属于羧酸 | |
| B. | 75%的酒精可以用于消毒,酒精的主要成分属于醇 | |
| C. | 聚乙烯可用于食品包装,聚乙烯属于烯烃 | |
| D. | 氟利昂是一种制冷剂,氟利昂属于卤代烃 |
3.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 24g镁的原子最外层电子数为NA | |
| B. | 0.3mol O2与一定量的Fe3+在一定条件下完全反应,生成Fe2O3和Fe3O4的混合物,则转移电子数为1.2mol | |
| C. | 2L 0.1mol/L氯化铁溶液中含有Fe的数目为0.2NA | |
| D. | 1L水中溶解了58.5gNaCl,该溶液的物质的量浓度为1mol/L |
13.下列关于化学用语的说法正确的是( )
| A. | Na+的结构示意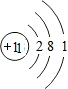 | |
| B. | CO2的结构式:O-C-O | |
| C. | CH4分子的比例模型为: | |
| D. | 用电子式表示氯化氢分子的形成过程:H•+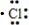 →H+[ →H+[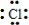 ]- ]- |
6.下列关于碳酸钠和碳酸氢钠的比较中,错误的是( )
| A. | 二者在一定的条件下可以相互转化 | |
| B. | 二者热稳定性不同,碳酸钠的热稳定性大于碳酸氢钠的热稳定性 | |
| C. | 等质量的碳酸钠与碳酸氢钠与足量盐酸反应,后者现象更剧烈,但前者产生的二氧化碳多 | |
| D. | 将二氧化碳通入到饱和碳酸钠溶液中,会有浑浊产生 |
3.下列离子方程式不正确的是( )
| A. | 乙酸与碳酸钠溶液反应:2 CH3COOH+CO32-→2CH3COO-+CO2↑+H2O | |
| B. | 苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | |
| C. | 醋酸溶液与新制氢氧化铜反应:2CH3COOH+Cu(OH)2→Cu2++2CH3COO-+2H2O | |
| D. | 乙醛溶液与足量的银氨溶液共热:CH3CHO+2[Ag(NH3)2]++2OH-$\stackrel{△}{→}$CH3COO-+NH4++2Ag↓+3NH3+H2O |
4.下列离子方程式正确的是( )
| A. | 浓硝酸中加入过量铁粉并加热:Fe+3NO3-+6H+$\frac{\underline{\;\;△\;\;}}{\;}$Fe3++3NO2↑+3H2O | |
| B. | 硫酸铜溶液与氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓ | |
| C. | 等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合:Ba2++2 OH-+NH4++HCO3-═BaCO3↓+NH3•H2O+H2O | |
| D. | 用FeCl3溶液腐蚀印刷电路板:Fe3++Cu═Fe2++Cu2+ |