题目内容
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、含有0.1 mol?L-1Fe3+的溶液中:K+、Mg2+、SCN-、SO42- |
| B、0.1 mol?L-1NaAlO2溶液:S2-、Na+、HCO3-、SO42- |
| C、能使酚酞变红的溶液:Na+、Ba2+、NO3-、Cl- |
| D、水电离产生的c(H+)=10-12mol?L-1的溶液中:Na+、Fe2+、SO42-、NO3- |
考点:离子共存问题
专题:离子反应专题
分析:A.含有0.1 mol?L-1Fe3+的溶液中,铁离子与硫氰根离子反应生成硫氰化铁;
B.0.1 mol?L-1NaAlO2溶液,碳酸氢根离子酸性大于氢氧化铝,碳酸氢根离子与偏铝酸根离子反应生成氢氧化铝沉淀;
C.能使酚酞变红的溶液为碱性溶液,Na+、Ba2+、NO3-、Cl-离子之间不反应,也不与氢氧根离子反应;
D.水电离产生的c(H+)=10-12mol?L-1的溶液中存在大量氢离子或者氢氧根离子,亚铁离子与氢氧根离子反应生成氢氧化亚铁.
B.0.1 mol?L-1NaAlO2溶液,碳酸氢根离子酸性大于氢氧化铝,碳酸氢根离子与偏铝酸根离子反应生成氢氧化铝沉淀;
C.能使酚酞变红的溶液为碱性溶液,Na+、Ba2+、NO3-、Cl-离子之间不反应,也不与氢氧根离子反应;
D.水电离产生的c(H+)=10-12mol?L-1的溶液中存在大量氢离子或者氢氧根离子,亚铁离子与氢氧根离子反应生成氢氧化亚铁.
解答:
解:A.含有0.1 mol?L-1Fe3+的溶液中,Fe3+与SCN-反应生成硫氰化铁,在溶液中不能大量共存,故A错误;
B.0.1 mol?L-1NaAlO2溶液,HCO3-与偏铝酸根离子反应生成氢氧化铝沉淀,在溶液中不能大量共存,故B错误;
C.能使酚酞变红的溶液中存在大量氢氧根离子,Na+、Ba2+、NO3-、Cl-离子之间不发生反应,且都不与氢氧根离子反应,在溶液中能够大量共存,故C正确;
D.水电离产生的c(H+)=10-12mol?L-1的溶液为酸性或者碱性溶液,Fe2+、与氢氧根离子反应生成氢氧化亚铁,在溶液中不能大量共存,故D错误;
故选C.
B.0.1 mol?L-1NaAlO2溶液,HCO3-与偏铝酸根离子反应生成氢氧化铝沉淀,在溶液中不能大量共存,故B错误;
C.能使酚酞变红的溶液中存在大量氢氧根离子,Na+、Ba2+、NO3-、Cl-离子之间不发生反应,且都不与氢氧根离子反应,在溶液中能够大量共存,故C正确;
D.水电离产生的c(H+)=10-12mol?L-1的溶液为酸性或者碱性溶液,Fe2+、与氢氧根离子反应生成氢氧化亚铁,在溶液中不能大量共存,故D错误;
故选C.
点评:本题考查离子共存的正误判断,为高考中的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;解决离子共存问题时还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等;试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
燃烧某混合气体,所产生的CO2的质量一定大于燃烧相同质量丙烯所产生的CO2的质量,该混合气体可以是( )
| A、丁烯、丙烷 |
| B、乙炔、乙烯 |
| C、乙炔、丙烷 |
| D、乙烷、丙烯 |
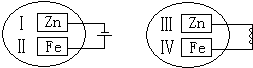 把锌片和铁片放在盛有稀食盐水和酚酞试液混合溶液的玻璃皿中(如图所示平面图),经过一段时间后,两个实验中,观察到的现象和对应方程式都正确的是( )
把锌片和铁片放在盛有稀食盐水和酚酞试液混合溶液的玻璃皿中(如图所示平面图),经过一段时间后,两个实验中,观察到的现象和对应方程式都正确的是( )| A、Ⅰ附近溶液变红,Zn-2e-=Zn2+ |
| B、Ⅳ附近溶液变红,O2+2H2O+4e-=4OH- |
| C、Ⅱ附近有黄绿色气体生成,2Cl--2e-=Cl2↑ |
| D、Ⅲ附近有无色气体生成,2H++2e-=H2↑ |
已知某温度下,0.1mol/LNaHCO3溶液中C(H+)<C(OH-)则下列关系一定不正确的是( )
| A、C(Na+)=C(HCOO-)+2 C(CO32-)+C(OH-) |
| B、C(H2CO3)+C(HCOO-)+C(CO32-)=0.1mol/L |
| C、将上述溶液稀释至0.01mol/L C(H+)×C(OH-)不变 |
| D、C(CO32-)+C(OH-)=C(H+)+C(H2CO3) |
 如图装置中,溶液体积均为200ml,开始时,电解质溶液的浓度均为0.1mol?L-1,工作一段时间后,测得导线上通过了0.02mol 电子,若不考虑溶液体积的变化,下列叙述中正确的是( )
如图装置中,溶液体积均为200ml,开始时,电解质溶液的浓度均为0.1mol?L-1,工作一段时间后,测得导线上通过了0.02mol 电子,若不考虑溶液体积的变化,下列叙述中正确的是( )| A、(1)、(2)两装置均为电解池 |
| B、(1)、(2)溶液的PH均减小 |
| C、(1)中阳极电极反应式为:4OH--4e-═2H2O+O2↑ |
| D、(1)中阴极上析出0.32 g Cu |
在盛有5mL饱和石灰水的试管中放入一小块钠,不可能观察到的现象是( )
| A、钠熔成小球并在液面上游动 |
| B、试管底部有银白色物质生成 |
| C、有气体生成 |
| D、溶液变浑浊 |
 准确称取6g铝土矿样品(含Al2O3、Fe2O3、SiO2),放入100mL浓度的H2SO4溶液中,充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生沉淀与加入NaOH溶液的体积的关系如图所示,
准确称取6g铝土矿样品(含Al2O3、Fe2O3、SiO2),放入100mL浓度的H2SO4溶液中,充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生沉淀与加入NaOH溶液的体积的关系如图所示,