题目内容
14.按要求填空(1)海水淡化的方法有蒸馏法、冰冻法、电渗析法、离子交换法、太阳能蒸发法等(至少两种);
(2)葡萄糖的结构简式CH2OH(CHOH ) 4CHO;
(3)火法炼铜的化学方程式Cu2S+O2$\frac{\underline{\;高温\;}}{\;}$2Cu+SO2;
(4)由CH3CH=CH2在催化剂条件下生成聚丙烯的化学方程式
 .
.
分析 (1)海水淡化海水就是将海水中的可溶性杂质除去的过程,可根据淡化原理进行分析解答;
目前淡化海水的方法有多种,如:蒸馏法、结晶法、淡化膜法、多级闪急蒸馏法等,其中最常用的是蒸馏法,据此解答;
(2)葡萄糖为多羟基醛,含有5个羟基一个醛基;
(3)火法炼铜原理为:高温下将硫化亚铜与氧气反应生成二氧化硫和铜;
(4)CH3CH=CH2在催化剂条件下生成聚丙烯,据此书写方程式.
解答 解:(1)解:目前淡化海水的方法有多种,如:蒸馏法、结晶法、淡化膜法、多级闪急蒸馏法等,其中最常用的是蒸馏法;
故答案为:蒸馏法、冰冻法、电渗析法、离子交换法、太阳能蒸发法;
(2)葡萄糖为多羟基醛,含有5个羟基一个醛基,结构简式为:CH2OH(CHOH ) 4CHO;
故答案为:CH2OH(CHOH ) 4CHO;
(3)火法炼铜原理为:高温下将硫化亚铜与氧气反应生成二氧化硫和铜,方程式:Cu2S+O2$\frac{\underline{\;高温\;}}{\;}$2Cu+SO2;
故答案为:Cu2S+O2$\frac{\underline{\;高温\;}}{\;}$2Cu+SO2;
(4)CH3CH=CH2在催化剂条件下生成聚丙烯,反应方程式: ;
;
故答案为: .
.
点评 本题考查了物质结构简式、化学方程式的书写,明确有机物结构是解题关键,题目难度中等.

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
4.下列说法正确的是( )
| A. | 淀粉、纤维素等高分子化合物均属于纯净物 | |
| B. | 金属氧化物都是碱性氧化物 | |
| C. | 食醋、纯碱、食盐分别属于酸、碱、盐 | |
| D. | 丁达尔效应可用于区别溶液与胶体 |
5.设NA为阿伏伽德罗常数的值,下列说法中正确的是( )
| A. | 常温常压下,16g CH4中含有的原子总数为5NA | |
| B. | 78g苯含有碳碳双键的数目为3NA | |
| C. | 1mol/L NaCl溶液中含有的氯离子数目为NA | |
| D. | 标准状态下,11.2L CH3COOH中含有的分子数目为0.5NA |
2.我国科学家首次拍摄到水分子团簇的空间取向图象(模型如图所示).下列关于水的说法不正确的是( )

| A. | 水分子间存在π键 | B. | 水分子间存在氢键 | ||
| C. | 水分子是V形结构 | D. | 水分子是极性分子 |
9.分子式为C8H16的某烯烃氢化后得到的饱和烃是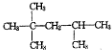 ,则该烯烃的结构最多有( )
,则该烯烃的结构最多有( )
 ,则该烯烃的结构最多有( )
,则该烯烃的结构最多有( )| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
19.下列化学式既能表示物质的组成,又能表示物质分子式的是( )
| A. | NH4NO3 | B. | SiO2 | C. | C6H5NO2 | D. | Cu |
6.下列四个图象中,反映出的对应变化关系错误的是( )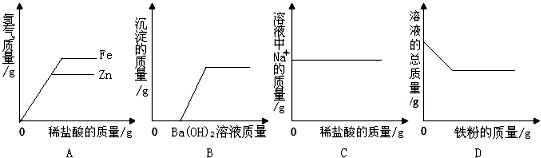

| A. | 将等质量的锌片和铁片分别加入足量的等质量等质量分数的稀盐酸中 | |
| B. | 向盐酸与硫酸钠混合溶液中加入氢氧化钡溶液 | |
| C. | 向一定量的氢氧化钠溶液中滴加稀盐酸 | |
| D. | 向一定量的硫酸铜溶液中加入铁粉 |
3.元素在周期表中的位置,反映了元素的原子结构和元素的性质,下列说法正确的是( )
| A. | 同一元素不可能既表现金属性,又表现非金属性 | |
| B. | 第三周期主族元素的最高正化合价等于它所处的主族序数 | |
| C. | 短周期元素原子形成简单离子后,最外层电子都达到8电子稳定结构 | |
| D. | 同一主族的元素的原子,最外层电子数相同,化学性质完全相同 |
5.科学研究表明,当前应用最广泛的化石燃料到本世纪中叶将枯竭,解决此危机的唯一途径是实现燃料和燃烧产物之间的良性循环(如图1).
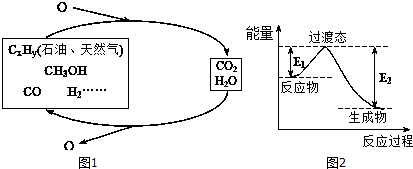
(1)一种常用的方法是在230℃、有催化剂条件下将CO2和H2转化为甲醇蒸汽和水蒸气.图2是生成1molCH3OH时的能量变化示意图.已知破坏1mol不同共价键的能量(kJ)分别是:
已知E1=8.2kJ•mol-1,则E2=198.8kJ•mol-1.
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行如下反应:CO(g)+H2O(g)?CO2(g)+H2(g),得到如下三组数据:
①该反应的△H<0(填“<”或“>”).
②实验2条件下的平衡常数K=1.
③实验3中,若平衡时H2O的转化率为$\frac{1}{3}$,则$\frac{a}{b}$=0.5,c=$\frac{b}{3}$.
④实验4,若900℃时,在容器中加入CO、H2O、CO2、H2各1mol,则此时V正=V逆(填“<”,“>”,“=”).
(3)捕捉CO2可以利用Na2CO3溶液,先用Na2CO3溶液吸收CO2生成NaHCO3,然后使NaHCO3分解,Na2CO3可以进行循环使用.将100mL0.1mol/LNa2CO3的溶液中通入112mL(已换算为标准状况)的CO2,溶液中没有晶体析出,则:
①反应后溶液中的各离子浓度由大到小的顺序是c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
②反应后的溶液可以作“缓冲液”(当往溶液中加入一定量的酸和碱时,有阻碍溶液pH变化的作用),请解释其原理如果向反应后的溶液中加入少量的酸时,碳酸根结合氢离子转化为碳酸氢根,溶液的PH变化不大,如果加入少量的碱时,碳酸氢根结合氢氧根转化为碳酸根,溶液的PH变化也不大,因此反应后溶液可以作缓冲液.

(1)一种常用的方法是在230℃、有催化剂条件下将CO2和H2转化为甲醇蒸汽和水蒸气.图2是生成1molCH3OH时的能量变化示意图.已知破坏1mol不同共价键的能量(kJ)分别是:
| C-H | C-O | C=O | H-H | H-O |
| 413.4 | 351 | 745 | 436 | 462.8 |
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行如下反应:CO(g)+H2O(g)?CO2(g)+H2(g),得到如下三组数据:
| 实验 | 温度/℃ | 起始量 | 达到平衡 | |||
| CO/mol | H2O/mol | H2/mol | CO转化率 | 所需时间/min | ||
| 1 | 650 | 4 | 2 | 1.6 | 6 | |
| 2 | 900 | 2 | 1 | 1/3 | 3 | |
| 3 | 900 | a | b | c | t | |
②实验2条件下的平衡常数K=1.
③实验3中,若平衡时H2O的转化率为$\frac{1}{3}$,则$\frac{a}{b}$=0.5,c=$\frac{b}{3}$.
④实验4,若900℃时,在容器中加入CO、H2O、CO2、H2各1mol,则此时V正=V逆(填“<”,“>”,“=”).
(3)捕捉CO2可以利用Na2CO3溶液,先用Na2CO3溶液吸收CO2生成NaHCO3,然后使NaHCO3分解,Na2CO3可以进行循环使用.将100mL0.1mol/LNa2CO3的溶液中通入112mL(已换算为标准状况)的CO2,溶液中没有晶体析出,则:
①反应后溶液中的各离子浓度由大到小的顺序是c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+).
②反应后的溶液可以作“缓冲液”(当往溶液中加入一定量的酸和碱时,有阻碍溶液pH变化的作用),请解释其原理如果向反应后的溶液中加入少量的酸时,碳酸根结合氢离子转化为碳酸氢根,溶液的PH变化不大,如果加入少量的碱时,碳酸氢根结合氢氧根转化为碳酸根,溶液的PH变化也不大,因此反应后溶液可以作缓冲液.