题目内容
两种金属组成的合金5.6g,与氯气完全反应,消耗氯气7.1g,则合金的组成可能( )
| A、Cu和Zn |
| B、Al和Zn |
| C、Al 和 Na |
| D、Cu和Fe |
考点:有关混合物反应的计算
专题:
分析:设金属为+2价,反应消耗金属的物质的量与氯气的物质的量相等,根据M=
计算出金属的平均摩尔质量,然后对各选项进行判断;注意+3价金属转化成+2价金属时的摩尔质量=原摩尔质量×
,+1价金属转化成+2价,其摩尔质量为原摩尔质量的2倍.
| m |
| n |
| 2 |
| 3 |
解答:
解:7.1g氯气的物质的量为
=0.1mol,
设金属为+2价,则金属的物质的量为0.1mol,混合金属的平均摩尔质量为:M=
=56g/mol,
A.铜的摩尔质量为64g/mol,锌的摩尔质量为65g/mol,二者摩尔质量都大于56g/mol,无法满足平均摩尔质量为56g/mol,故A错误;
B.Al+2价时摩尔质量为:
×2=18g/mol,锌的摩尔质量为65g/mol,二者的平均摩尔质量可以为56g/mol,故B正确;
C.Al+2价时摩尔质量为:
×2=18g/mol,钠为+2价的摩尔质量为:23g/mol×2=46g/mol,二者的摩尔质量都小于56g/mol,故C错误;
D.铁的+2的摩尔质量为:56g/mol×
≈37.3,铜的摩尔质量为64g/mol,二者的平均摩尔质量可以为56g/mol,故D正确;
故选BD.
| 7.1g |
| 71g/mol |
设金属为+2价,则金属的物质的量为0.1mol,混合金属的平均摩尔质量为:M=
| 5.6g |
| 0.1mol |
A.铜的摩尔质量为64g/mol,锌的摩尔质量为65g/mol,二者摩尔质量都大于56g/mol,无法满足平均摩尔质量为56g/mol,故A错误;
B.Al+2价时摩尔质量为:
| 27g/mol |
| 3 |
C.Al+2价时摩尔质量为:
| 27g/mol |
| 3 |
D.铁的+2的摩尔质量为:56g/mol×
| 2 |
| 3 |
故选BD.
点评:本题考查了有关混合金属反应的化学计算,题目难度中等,注意掌握平均摩尔质量法在化学计算中的应用,试题侧重考查学生的分析、理解能力及化学计算能力.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
可用来提取含有杂质Br2的溴苯的试剂是( )
| A、水 | B、酒精 |
| C、NaOH溶液 | D、苯 |
在碱性溶液中能大量共存且为无色透明溶液的是( )
| A、K+ Cl- MnO4- SO42- |
| B、Ca2+ CO32- NO3- SO42- |
| C、Na+ HCO3- NO3- SO42- |
| D、Na+ SO42- NO3- Cl- |
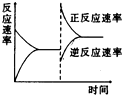 如图是改变某一外界条件后反应A2(s)+3B2(g)?2C(g)△H<0的反应速率与时间图象,则改变的条件可能是( )
如图是改变某一外界条件后反应A2(s)+3B2(g)?2C(g)△H<0的反应速率与时间图象,则改变的条件可能是( )| A、升高温度,同时加压 |
| B、保持体系压强不变加入反应物A2 |
| C、降低温度,同时减压 |
| D、保持体系压强不变加入反应物B2 |
有下列物质:①白磷;②金刚石;③石墨;④二氧化硅;⑤甲烷;⑥四氯化碳;⑦单质硅;⑧铵根离子.其分子结构或晶体结构单元中存在正四面体的是( )
| A、除③外 | B、①②⑤⑥ |
| C、除③⑧外 | D、除③④⑦⑧ |
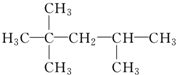 的名称是
的名称是