题目内容
【题目】往含0.2mol NaOH和0.1mol Ca(OH)2的溶液中持续稳定地通入CO2气体,当通入气体为6.72L(S.T.P)时立即停止,则这一过程中,溶液中离子的物质的量和通入CO2气体的体积关系正确的图象是(气体的溶解忽略不计)( )
A.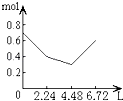
B.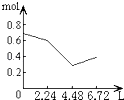
C.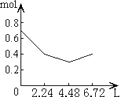
D.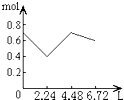
【答案】C
【解析】解:n(CO2)= ![]() =0.3mol, 含有0.2mol氢氧化钠和0.1mol氢氧化钙的溶液中:n(OH﹣)=0.2mol+0.1mol×2=0.4mol,n(Na+)=0.2mol,
=0.3mol, 含有0.2mol氢氧化钠和0.1mol氢氧化钙的溶液中:n(OH﹣)=0.2mol+0.1mol×2=0.4mol,n(Na+)=0.2mol,
n(Ca2+)=0.1mol,
通入CO2 , 发生:2OH﹣+CO2=CO32﹣+H2O,OH﹣+CO2=HCO3﹣+H2O,Ca2++CO32﹣=CaCO3↓,
设生成xmolCO32﹣ , ymolHCO3﹣ ,
则 ![]() ,解得x=0.1,y=0.2,
,解得x=0.1,y=0.2,
通入含有0.2molNaOH和0.1molBa(OH)2的溶液中,相当于首先发生:Ba2++2OH﹣+CO2=BaCO3↓,该阶段0.1molBa(OH)2完全反应消耗0.1molCO2 , 体积为2.24L,离子物质的量减少0.3mol,溶液中离子物质的量为0.7mol﹣0.3mol=0.4mol,其中含有0.2molOH﹣、生成0.1molBaCO3;
然后发生2OH﹣+CO2=CO32﹣+H2O,0.2molOH﹣完全反应消耗0.1molCO2 , 体积为2.24L,该阶段离子物质的量减少0.1mol,溶液中剩余离子物质的量为0.4mol﹣0.1mol=0.3mol,溶液中含有0.2molNa+、0.1molCO32﹣;
再发生CO32﹣+CO2+H2O=2HCO3﹣、BaCO3+CO2+H2O=Ba2++2HCO3﹣ , 消耗0.1molCO2 , 体积为2.24L,溶液中离子物质的量增大,溶液中离子为0.6mol,
所以图象C符合,
故选C.
n(CO2)= ![]() =0.3mol,通入含有0.2mol氢氧化钠和0.1mol氢氧化钙的溶液中,发生:2OH﹣+CO2=CO32﹣+H2O,OH﹣+CO2=HCO3﹣+H2O,Ca2++CO32﹣=CaCO3↓,以此解答该题.
=0.3mol,通入含有0.2mol氢氧化钠和0.1mol氢氧化钙的溶液中,发生:2OH﹣+CO2=CO32﹣+H2O,OH﹣+CO2=HCO3﹣+H2O,Ca2++CO32﹣=CaCO3↓,以此解答该题.