题目内容
2.与100mL0.1mol/L(NH4)2SO4中的c(NH4+)相同的溶液是( )| A. | 200mL 0.1mol/L NH4Cl溶液 | B. | 50mL 0.2mol/L NH4NO3溶液 | ||
| C. | 100mL 0.2mol/L NH3•H2O溶液 | D. | 100mL 0.2mol/L (NH4)2SO3溶液 |
分析 根据溶液中不水解的离子的物质的量浓度=溶质的物质的量浓度×化学式中离子的个数进行计算NO3-的物质的量浓度,与溶液的体积无关,100mL0.1mol/L(NH4)2SO4溶液中NH4+物质的量浓度=0.1mol/L×2=0.2mol/L,以此解答该题.
解答 解:100mL0.1mol/L(NH4)2SO4溶液中NH4+物质的量浓度为0.2mol/L,
A.200mL 0.1mol/L NH4Cl溶液中NH4+物质的量浓度为0.1mol/L;
B.50mL 0.2mol/L NH4NO3溶液中NH4+物质的量浓度为0.2mol/L;
C.NH3•H2O为弱电解质,部分电离,NH4+物质的量浓度小于0.2mol/L
D.100mL 0.2mol/L (NH4)2SO3溶液中NH4+物质的量浓度为0.4mol/L,
故选B.
点评 本题考查了离子浓度的计算,为高频考点,明确“溶液中不水解的离子的物质的量浓度=溶质的物质的量浓度×化学式中离子的个数进行计算氯离子的物质的量浓度,与溶液的体积无关”是解本题的关键,难度不大.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
13.下列说法正确的是( )
| A. | 由H原子形成1molH-H键要吸收热量 | |
| B. | 化学变化中的能量变化的大小与反应物的质量多少无关 | |
| C. | 酸与碱的稀溶液发生中和反应生成1molH2O时所释放的热量称为中和热 | |
| D. | 锌锰干电池中碳棒是负极,锌片是正极 |
7.Ca(ClO)2是漂白粉的有效成分.用漂白粉漂白时,不能使漂白粉更好发挥漂白作用的物质是( )
| A. | 酒精 | B. | CO2和水蒸汽 | C. | 盐酸 | D. | 食醋(含CH3COOH) |
14.能源可划分为一级能源和二级能源,自然界以现成方式提供的能源称为一级能源;需依靠其他能源的能量间接制取的能源称为二级能源.氢气是一种高效而没有污染的二级能源,它可以由自然界中大量存在的水来制取;未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生.下列叙述正确的是( )
| A. | 水煤气,电能是一级能源 | |
| B. | 天然气,水力是二级能源 | |
| C. | 核能,煤,石油符合未来新能源标准 | |
| D. | 太阳能,生物质能,风能,氢能符合未来新能源标准 |
11.下列变化过程中,没有破坏化学键的是( )
| A. | 氯化钠的融化 | B. | 乙醇溶于水 | C. | 乙烯的燃烧 | D. | 水的通电分解 |
12.下列关于碱金属的叙述,正确的是( )
| A. | 金属钠着火时,可用水或泡沫灭火器灭火 | |
| B. | 碱金属单质都可保存在煤油中 | |
| C. | 钠离子半径比钠原子半径小 | |
| D. | 碱金属中密度最小,熔、沸点最高的是铯 |
 ,
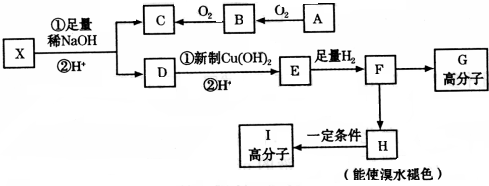
,
 .
. .
. .
.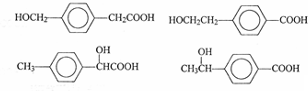 .
.