题目内容
17.常温下,下列各组离子在指定溶液中一定能大量共存的是( )| A. | 使甲基橙变红色的溶液中; K+、Ba2+、AlO2-、NO3- | |
| B. | 1.0mol/L的KI溶液中:Na+、Fe3+、Cl-、SO42- | |
| C. | 与铝反应产生大量氢气的溶液中:Mg2+、HCO3-、Cl-、NO3- | |
| D. | c(H+)=1×10-13mol/L溶液中:Na+、AlO2-、SiO32-、PO43- |
分析 A.使甲基橙变红色的溶液,显酸性;
B.离子之间发生氧化还原反应;
C.与铝反应产生大量氢气的溶液,为非氧化性酸或强碱溶液;
D.c(H+)=1×10-13mol/L溶液,显碱性.
解答 解:A.使甲基橙变红色的溶液,显酸性,不能大量存在AlO2-,故A错误;
B.Fe3+、I-发生氧化还原反应,不能共存,故B错误;
C.与铝反应产生大量氢气的溶液,为非氧化性酸或强碱溶液,酸碱溶液中均不能大量存在HCO3-,碱溶液中也不能大量存在Mg2+,故C错误;
D.c(H+)=1×10-13mol/L溶液,显碱性,该组离子之间不反应,可大量共存,故D正确;
故选D.
点评 本题考查离子共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意氧化还原反应、复分解反应的判断,题目难度不大.

练习册系列答案
相关题目
8.化学与生产、生活、社会密切相关.下列有关说法中不正确的是( )
| A. | 2009年12月在哥本哈根召开的国际气候会议受到全球政要的广泛关注.减缓工业生产大量二氧化硫的排放以抑制全球气候变暖成为该会议的主题 | |
| B. | 针对目前甲型H1N1流感的扩散情况,要加强对环境、个人的消毒预防.其中消毒剂常选用含氯消毒剂、酒精、双氧水等适宜的物质 | |
| C. | 2009年诺贝尔物理学奖授予华裔科学家高锟,是因其在光纤材料领域取得了卓越贡献.光纤的主要成分与玛瑙相同,通常情况下不与强氧化剂和强酸反应 | |
| D. | 建国60周年庆典晚会上,天安门广场燃放的焰火是某些金属元素魅力的展现 |
5.下列说法正确的是( )
| A. | 28g N2含有的原子数为NA | |
| B. | 4gCa变成Ca2+失去的电子数为0.1NA | |
| C. | 1molO2的质量等于1mol O的质量 | |
| D. | 24gO2和24gO3所含有的原子数目相等 |
12.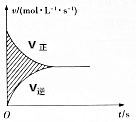 在容积为4L的刚性密闭容器中,进行可逆反应:X(g)+2Y(g)?2Z(g)并达到平衡,在此过程中以Y的浓度改变表示的反应速率v正、v逆与时间t的关系如图所示,则图中阴影部分的面积表示( )
在容积为4L的刚性密闭容器中,进行可逆反应:X(g)+2Y(g)?2Z(g)并达到平衡,在此过程中以Y的浓度改变表示的反应速率v正、v逆与时间t的关系如图所示,则图中阴影部分的面积表示( )
 在容积为4L的刚性密闭容器中,进行可逆反应:X(g)+2Y(g)?2Z(g)并达到平衡,在此过程中以Y的浓度改变表示的反应速率v正、v逆与时间t的关系如图所示,则图中阴影部分的面积表示( )
在容积为4L的刚性密闭容器中,进行可逆反应:X(g)+2Y(g)?2Z(g)并达到平衡,在此过程中以Y的浓度改变表示的反应速率v正、v逆与时间t的关系如图所示,则图中阴影部分的面积表示( )| A. | X的浓度的变化量 | B. | Y的浓度的减小量 | ||
| C. | Z的物质的量的变化量 | D. | Y的物质的量的减小量 |
6.在指定的条件下,下列各组离子一定能大量共存的是( )
| A. | 无色的溶液中:Fe3+、K+、NO3-、Cl- | |
| B. | 含有大量Ba2+的溶液中:NH4+、Na+、Cl-、H+ | |
| C. | pH=13的溶液中:NH4+、Na+、SO42-、Cl- | |
| D. | c(H+)=0.1 mol•L-1的溶液中:K+、I-、Cl-、NO3- |
16.下列属于吸热反应的是( )
| A. | 锌粒与稀硫酸反应 | B. | 盐酸与氢氧化钠反应 | ||
| C. | 液化石油气的燃烧 | D. | 石灰石高温分解 |
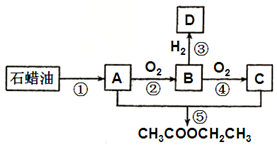 烃A是一种重要的化工原料.已知A在标准状况下的密度为1.25g•L-1,B可发生银镜反应.它们之间的转化关系如图:
烃A是一种重要的化工原料.已知A在标准状况下的密度为1.25g•L-1,B可发生银镜反应.它们之间的转化关系如图:
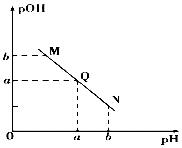 现有①0.1mol/L NaOH溶液和②0.1mol/L HX溶液.
现有①0.1mol/L NaOH溶液和②0.1mol/L HX溶液.