题目内容
14.对于数以万计的化学物质和化学反应,分类法的作用几乎是无可替代的.(1)现有下列5种物质:CuO、CO、MgO、Na2O、FeO.按照不同的分类标准,它们中有1种物质与其他4种物质有明显的不同,找出这种物质,并写出依据(写出两种):
①CO;常温常压下是气体,其余是固体;
②CO;非金属氧化物,其余是金属氧化物.
(2)虽然分类的方法不同,但离子反应和氧化还原反应之间也存在着一定的关系,用简单的图示方法表示二者之间的关系
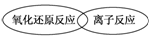 .
.(3)生活中的食醋和豆浆分别属于分散系中的溶液和胶体,用丁达尔效应可以鉴别(填化学专用名词).
分析 (1)找出不同类的物质,要抓住其余5种物质的共同点,可以从物理性质和化学性质两方面进行分析;
(2)离子反应有的是氧化还原反应,有的不是氧化还原反应;
(3)食醋属于溶液,淀粉溶液属于胶体,丁达尔效应是胶体的特性;
解答 解:(1)①根据物质的状态分析,CO为气体,其余为固体,
故答案为:CO;常温常压下是气体,其余是固体;
②根据物质组成和状态来分类,在CuO、CO、MgO、Na2O、FeO中,CO属于非金属氧化物,CuO、MgO、Na2O、FeO属于金属氧化物,
故答案为:CO;非金属氧化物,其余是金属氧化物;
(2)离子反应有的是氧化还原反应,有的不是氧化还原反应,二者的关系可以用右图表示: ,如离子反应H++OH-=H2O不属于氧化还原反应,离子反应Cl2+H2O=H++Cl-+HClO属于氧化还原反应,
,如离子反应H++OH-=H2O不属于氧化还原反应,离子反应Cl2+H2O=H++Cl-+HClO属于氧化还原反应,
故答案为:; ;
;
(3)食醋属于溶液,淀粉溶液属于胶体,溶液无丁达尔效应,胶体有丁达尔效应,
故答案为:溶液;胶体;丁达尔效应.
点评 本题考查了物质的分类以及氧化还原反应的特征、方程式的书写、胶体的鉴别,该考点的基础性比较强,主要出现在选择题和填空题中,题目难度不大.

练习册系列答案
相关题目
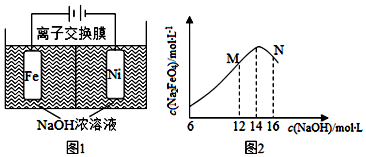
2. 人工肾脏可用间接电化学方法除去代谢产物中的尿素[CO(NH2)2],原理如图.下列有关说法正确的是( )
人工肾脏可用间接电化学方法除去代谢产物中的尿素[CO(NH2)2],原理如图.下列有关说法正确的是( )
 人工肾脏可用间接电化学方法除去代谢产物中的尿素[CO(NH2)2],原理如图.下列有关说法正确的是( )
人工肾脏可用间接电化学方法除去代谢产物中的尿素[CO(NH2)2],原理如图.下列有关说法正确的是( )| A. | A为电源的负极 | |
| B. | 电解结束后,阴极室溶液的pH与电解前相比将不变 | |
| C. | 阳极室中发生的电极反应为2H++2e-═H2↑ | |
| D. | 若两极共收集到气体13.44 L(标准状况),则除去的尿素为18g(忽略气体的溶解) |
6.下列分子中心原子均是sp2杂化的是( )
| A. | PBr3、NO2 | B. | CH4、SCl2 | C. | BF3、SO2 | D. | H2O、CS2 |
3.微量元素在人体内含量极少,但它们对于维持生命活动,促进人体健康生长和发育都有极其重要的作用.下列元素中,若缺乏严重会导致智力损害的是( )
| A. | 钙元素 | B. | 碘元素 | C. | 铁元素 | D. | 钠元素 |
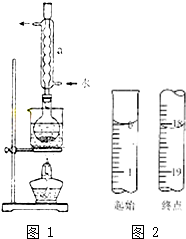
16.己二酸是合成尼龙-66的主要原料之一.实验室合成己二酸的原理、有关数据及装置示意图为: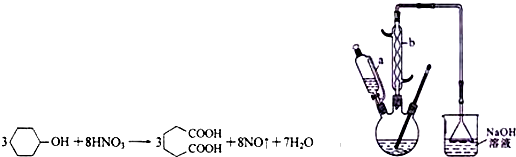
实验步骤如下:
Ⅰ.在三口烧瓶中加入16mL50%的硝酸(密度为1.31g/cm3),再加入1~2粒沸石,滴液漏斗中盛放有5.4mL环己醇.
Ⅱ.水浴加热三口烧瓶至50℃左右,移去水浴,缓慢滴加5~6滴环己醇,摇动三口烧瓶,观察到有红棕色
气体放出时再慢慢滴加剩下的环己醇,维持反应温度在60℃~65℃之间.Ⅲ.当环己醇全部加入后,将混合物用80℃~90℃水浴加热约10min(注意控制温度),直至无红棕色气体生成为止.
Ⅳ.趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤、干燥、称重.
请回答下列问题:
(1)装置中仪器b的名称为球形冷凝管(或冷凝管),使用时要从下口(填“上口”或“下口”)通入冷水;滴液漏斗的细支管a的作用是平衡滴液漏斗与三口烧瓶内的气压,使环己醇能够顺利流下.
(2)本实验所用50%的硝酸的物质的量浓度为10.4mol/L;NaOH溶液的作用是吸收NO2,防止污染空气.
(3)向三口烧瓶中滴加环己醇时,反应温度迅速上升,为使反应温度不致过高,必要时可采取的措施是将三口烧瓶置于冷水浴中.
(4)为了除去可能的杂质和减少产品损失,可依次用冷水和苯洗涤晶体.
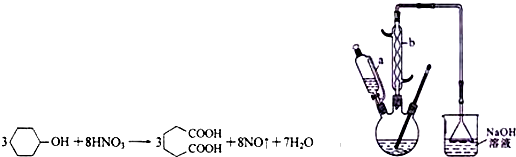
| 物质 | 密度(20℃) | 熔点 | 沸点 | 溶解性 |
| 环己醇 | 0.962g/cm3 | 25.9℃ | 160.8℃ | 20℃时水中溶解度为3.6g,可混溶于乙醇、苯 |
| 己二酸 | 1.360g/cm3 | 152℃ | 337.5℃ | 在水中的溶解度:15℃时1.44g,25℃时2.3g,易溶于乙醇、不溶于苯 |
Ⅰ.在三口烧瓶中加入16mL50%的硝酸(密度为1.31g/cm3),再加入1~2粒沸石,滴液漏斗中盛放有5.4mL环己醇.
Ⅱ.水浴加热三口烧瓶至50℃左右,移去水浴,缓慢滴加5~6滴环己醇,摇动三口烧瓶,观察到有红棕色
气体放出时再慢慢滴加剩下的环己醇,维持反应温度在60℃~65℃之间.Ⅲ.当环己醇全部加入后,将混合物用80℃~90℃水浴加热约10min(注意控制温度),直至无红棕色气体生成为止.
Ⅳ.趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤、干燥、称重.
请回答下列问题:
(1)装置中仪器b的名称为球形冷凝管(或冷凝管),使用时要从下口(填“上口”或“下口”)通入冷水;滴液漏斗的细支管a的作用是平衡滴液漏斗与三口烧瓶内的气压,使环己醇能够顺利流下.
(2)本实验所用50%的硝酸的物质的量浓度为10.4mol/L;NaOH溶液的作用是吸收NO2,防止污染空气.
(3)向三口烧瓶中滴加环己醇时,反应温度迅速上升,为使反应温度不致过高,必要时可采取的措施是将三口烧瓶置于冷水浴中.
(4)为了除去可能的杂质和减少产品损失,可依次用冷水和苯洗涤晶体.
 Na2S2O3是重要的化工原料,易溶于水.在中性或碱性环境中稳定.
Na2S2O3是重要的化工原料,易溶于水.在中性或碱性环境中稳定. ,该反应属于取代(填“取代”或“加成”)反应.
,该反应属于取代(填“取代”或“加成”)反应.