题目内容
2.下列与化学反应速率的影响因素无关的是( )| A. | 建筑中使用的铝合金门窗比钢门窗更耐腐蚀 | |
| B. | 窗帘上直接受阳光照射的一面布料容易褪色 | |
| C. | 肉放在冷冻箱中要比放在保鲜箱中存放的时间更长久 | |
| D. | 实验室用硫酸溶液与锌粒反应制取氢气,反应一段时间后,气泡变得稀少了(锌粒还有剩余),如果添加一些适当浓度的硫酸溶液到反应容器中,气泡又重新增多起来 |
分析 A.铝合金门窗比钢门窗更耐腐蚀,与合金的性质有关;
B.光照射,温度升高;
C.冷冻箱中要比放在保鲜箱中存放的时间更长久,温度降低,反应速率减小;
D.添加一些适当浓度的硫酸溶液,氢离子浓度增大.
解答 解:A.铝合金门窗比钢门窗更耐腐蚀,与合金的性质有关,与反应速率无关,故A选;
B.光照射,温度升高,加快氧化速率,故B不选;
C.冷冻箱中要比放在保鲜箱中存放的时间更长久,温度降低,反应速率减小,与温度对反应速率的影响有关,故C不选;
D.添加一些适当浓度的硫酸溶液,氢离子浓度增大,反应速率加快,与浓度对反应速率的影响有关,故D不选;
故选A.
点评 本题考查化学反应速率的影响因素,为高频考点,把握温度、浓度对反应速率的影响为解答的关键,侧重分析与应用能力的考查,注意合金的性质,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12. 甲醇是重要的化工原料,又可作为燃料.工业上利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
甲醇是重要的化工原料,又可作为燃料.工业上利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g)?CH3OH(g)△H=-99kJ/mol
②CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-58kJ/mol
③CO2(g)+H2(g)?CO(g)+H2O(g)△H=+41kJ/mol
回答下列问题:
(1)已知反应①中相关的化学键键能数据如表:
则x=413.
(2)反应①能够自发进行的条件是较低温度(填“较低温度”、“较高温度”或“任何温度”).
(3)恒温,恒容密闭容器中,对于反应②,下列说法中能说明该反应达到化学平衡状态的是BD.
A.混合气体的密度不再变化
B.混合气体的平均相对分子质量不再变化
C.CO2、H2、CH3OH、H2O的物质的量之比为1:3:1:1
D.甲醇的百分含量不再变化
(4)对于反应②,不同温度对CO2的转化率及催化剂的效率影响如图所示,下列有关说法
不正确的是ABD.
A.不同条件下反应,N点的速率最大
B.温度低于250℃时,随温度升高甲醇的产率增大
C.M点时平衡常数比N点时平衡常数大
D.实际反应应尽可能在较低的温度下进行,以提高CO2的转化率
(5)若在1L密闭容器中充入体积比为 3:1的 H2 和CO2发生反应②,则图中M点时,产物甲醇的体积分数为16.7%;若要进一步提高甲醇的体积分数,可采取的措施有增大压强(答一种措施).
(6)甲醇在催化剂条件下可以直接氧化成甲酸.常温下用0.1000mol•L-1NaOH滴定 20.00mL 0.1000mol•L-1的甲酸.当溶液中c(HCOOH)=c(HCOO-)时,测得PH=4.
①PH=4时,该溶液中离子浓度由小到大的顺序为c(OH-)<c(H+)<c(Na+)<c(HCOO-);
②PH=7时,c(HCOOH)+c(HCOO-)>0.050mol•L-1(填“>”、“<”或“=”)
 甲醇是重要的化工原料,又可作为燃料.工业上利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
甲醇是重要的化工原料,又可作为燃料.工业上利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:①CO(g)+2H2(g)?CH3OH(g)△H=-99kJ/mol
②CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-58kJ/mol
③CO2(g)+H2(g)?CO(g)+H2O(g)△H=+41kJ/mol
回答下列问题:
(1)已知反应①中相关的化学键键能数据如表:
| 化学键 | H-H | C-O | C≡O | H-O | C-H |
| E/(KJ•mol-1) | 436 | 343 | 1076 | 465 | x |
(2)反应①能够自发进行的条件是较低温度(填“较低温度”、“较高温度”或“任何温度”).
(3)恒温,恒容密闭容器中,对于反应②,下列说法中能说明该反应达到化学平衡状态的是BD.
A.混合气体的密度不再变化
B.混合气体的平均相对分子质量不再变化
C.CO2、H2、CH3OH、H2O的物质的量之比为1:3:1:1
D.甲醇的百分含量不再变化
(4)对于反应②,不同温度对CO2的转化率及催化剂的效率影响如图所示,下列有关说法
不正确的是ABD.
A.不同条件下反应,N点的速率最大
B.温度低于250℃时,随温度升高甲醇的产率增大
C.M点时平衡常数比N点时平衡常数大
D.实际反应应尽可能在较低的温度下进行,以提高CO2的转化率
(5)若在1L密闭容器中充入体积比为 3:1的 H2 和CO2发生反应②,则图中M点时,产物甲醇的体积分数为16.7%;若要进一步提高甲醇的体积分数,可采取的措施有增大压强(答一种措施).
(6)甲醇在催化剂条件下可以直接氧化成甲酸.常温下用0.1000mol•L-1NaOH滴定 20.00mL 0.1000mol•L-1的甲酸.当溶液中c(HCOOH)=c(HCOO-)时,测得PH=4.
①PH=4时,该溶液中离子浓度由小到大的顺序为c(OH-)<c(H+)<c(Na+)<c(HCOO-);
②PH=7时,c(HCOOH)+c(HCOO-)>0.050mol•L-1(填“>”、“<”或“=”)
13.取一定质量的铜片和一定体积的浓硫酸放在烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,若要使铜片继续溶解可向烧瓶中加入( )
| A. | 稀H2SO4 | B. | 稀盐酸 | C. | K2SO4固体 | D. | KNO3固体 |
10.下列说法正确的是( )
| A. | 等物质的量的O2和O3含有相同的质子数 | |
| B. | 水是一种非常稳定的化合物,这是由于氢键所致 | |
| C. | 分子晶体中一定存在分子间作用力,但可能没有共价键 | |
| D. | 将标准状况下22.4 L 氨气溶于1 L水配成溶液,可得1 mol•L-1的氨水 |
17.设NA为阿伏加德罗常数值.下列有关叙述正确的是( )
| A. | 1 mol D2O分子所含的中子数为8NA | |
| B. | 48 g氧气和臭氧的混合气体中的氧原子数为3NA | |
| C. | 11.2 L 甲烷(CH4)中的共价键数为2NA | |
| D. | 1 mol N2与3 mol H2反应生成的NH3分子数为2NA |
7.将1一氯丙烷跟NaOH的醇溶液共热,生成的产物再跟溴的四氯化碳溶液反应,得到一种有机物,它的同分异构体有(除它之外)( )
| A. | 2 种 | B. | 3 种 | C. | 4 种 | D. | 5 种 |
14. 已知某化学反应A2(g)+2B2(g)═2AB2(g)(A2、B2、AB2的结构式分别为 A═A、B-B、B-A-B),能量变化如图所示,下列有关叙述中正确的是( )
已知某化学反应A2(g)+2B2(g)═2AB2(g)(A2、B2、AB2的结构式分别为 A═A、B-B、B-A-B),能量变化如图所示,下列有关叙述中正确的是( )
 已知某化学反应A2(g)+2B2(g)═2AB2(g)(A2、B2、AB2的结构式分别为 A═A、B-B、B-A-B),能量变化如图所示,下列有关叙述中正确的是( )
已知某化学反应A2(g)+2B2(g)═2AB2(g)(A2、B2、AB2的结构式分别为 A═A、B-B、B-A-B),能量变化如图所示,下列有关叙述中正确的是( )| A. | 该反应的进行一定需要加热或点燃条件 | |
| B. | 该反应若生成2molAB2(g)则放出的热量为 (E1-E2) kJ | |
| C. | 该反应断开化学键消耗的总能量大于形成化学键释放的总能量 | |
| D. | 生成2 mol B-A键放出E2 kJ能量 |
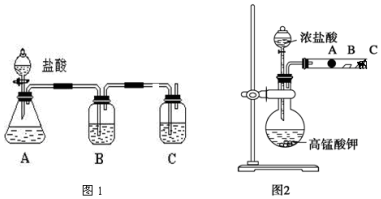
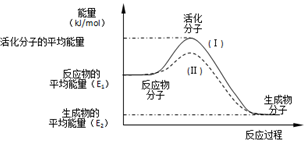 在化学反应中,只有极少数分子的能量比所有分子的平均能量高得多,只有这些高能量的分子发生碰撞时才可能发生化学反应,人们把这些高能量的分子称为活化分子,其他分子成为普通分子.把活化分子的平均能量与反应物分子的平均能量之间的差值叫活化能,单位为kJ/mol.请认真观察如图后回答问题.
在化学反应中,只有极少数分子的能量比所有分子的平均能量高得多,只有这些高能量的分子发生碰撞时才可能发生化学反应,人们把这些高能量的分子称为活化分子,其他分子成为普通分子.把活化分子的平均能量与反应物分子的平均能量之间的差值叫活化能,单位为kJ/mol.请认真观察如图后回答问题.