题目内容
17.设NA为阿伏加德罗常数值.下列有关叙述正确的是( )| A. | 1 mol D2O分子所含的中子数为8NA | |
| B. | 48 g氧气和臭氧的混合气体中的氧原子数为3NA | |
| C. | 11.2 L 甲烷(CH4)中的共价键数为2NA | |
| D. | 1 mol N2与3 mol H2反应生成的NH3分子数为2NA |
分析 A.1个D2O分子中含中子数为:1×2+8=10;
B.氧气和臭氧都是由氧原子构成;
C.气体状况未知;
D.合成氨为可逆反应,不能进行到底.
解答 解:A.1 mol D2O分子所含的中子数为10NA,故A错误;
B.48 g氧气和臭氧的混合气体中的氧原子数为:$\frac{48g}{16g/mol}$×NA=3NA,故B正确;
C.气体状况未知,无法计算甲烷的物质的量和共价键数,故C错误;
D.合成氨为可逆反应,不能进行到底,所以1 mol N2与3 mol H2反应生成的NH3分子数小于2NA,故D错误;
故选:B.
点评 本题考查阿伏加德罗常数的有关计算和判断,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确气体摩尔体积使用条件和对象是解题关键,题目难度中等.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案
相关题目
8.铷元素(Rb)位于元素周期表中第五周期第ⅠA族,有关Rb及其化合物的性质推测正确的是( )
| A. | Rb与冷水反应比K更剧烈 | B. | Rb投入CuSO4溶液中可置换出Cu | ||
| C. | Rb与O2反应只有Rb2O产生 | D. | Rb2CO3难溶于水 |
5.下列各组物质含有的化学键类型完全相同的是( )
| A. | HBr、CO2、NH3 | B. | Na2O、Na2O2、Na2S | C. | NaCl、HCl、H2O | D. | NaOH、CaCl2 CaO |
2.下列与化学反应速率的影响因素无关的是( )
| A. | 建筑中使用的铝合金门窗比钢门窗更耐腐蚀 | |
| B. | 窗帘上直接受阳光照射的一面布料容易褪色 | |
| C. | 肉放在冷冻箱中要比放在保鲜箱中存放的时间更长久 | |
| D. | 实验室用硫酸溶液与锌粒反应制取氢气,反应一段时间后,气泡变得稀少了(锌粒还有剩余),如果添加一些适当浓度的硫酸溶液到反应容器中,气泡又重新增多起来 |
9.通常情况下,氣化钠、氯化铯、二氧化碳和二氧化硅的晶体结构分别如图所示:
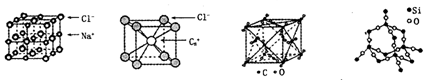
下列关于这些晶体结构和性质的叙述不正确的是( )

下列关于这些晶体结构和性质的叙述不正确的是( )
| A. | 同一主族的元素与另一相同元素所形成的化学式相似的物质不一定具有相同 的晶体结构 | |
| B. | 氯化钠、氯化铯和二氧化碳的晶体都有立方的晶胞结构,它们具有相似物理 性质 | |
| C. | 二氧化碳晶体是分子晶体,其中不仅存在分子间作用力,而且也存在共价键 | |
| D. | 二氧化硅晶体不是密堆积结构 |
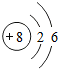 ,b的最简单氢化物的电子式为
,b的最简单氢化物的电子式为 .
. .
.