题目内容
【题目】我国采用的Cu2O/TiO2–NaBiO3光催化氧化技术能深度净化工业含有机物的废水。回答下列问题:
(1)钛(Ti)的基态原子M能层中能量不同的电子有_____________种。
(2)该技术能有效将含有机物废水中的农药、醇、油等降解为水、二氧化碳、硝酸根离子等小分子。
①H2O、CH3OH、![]() 分子中O-H键的极性最强的是_____________。
分子中O-H键的极性最强的是_____________。
②C、N、O三种元素的电负性由大到小的顺序是_____________。
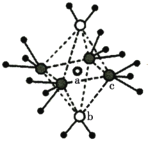
(3)将少量无水硫酸铜溶解在水中,形成蓝色溶液,再加入过量氨水,溶液变为深蓝色。深蓝色离子的结构如图所示,lmol该离子中所含σ键为_____________mol(包括配位键);向深蓝色溶液中缓慢加入乙醇,得到深蓝色晶体,加热该晶体先失去组分b的原因是_____________。
(4)铋合金具有凝固时不收缩的特性,用于铸造高精度铸型。金属铋的结构示意图如图1所示,其晶胞结构如图2所示。若铋原子的半径为rpm,则该晶体的密度为_____________gcm-3 (用含r和NA数学表达式表示)。

【答案】3 ![]() O>N>C 22 NH3与Cu2+的配位能力比H2O强
O>N>C 22 NH3与Cu2+的配位能力比H2O强 ![]() ×1030
×1030
【解析】
(1)钛(Ti)的基态原子核外电子排布为1s22s22p63s23p63d24s2,据此分析解答;
(2)①电离难易程度与极性关系,一般极性越大,越容易电离;
②同周期元素,随核电荷数增大,电负性逐渐增强;
(3)单键和配位键都为σ键,根据图示分析判断;乙醇为极性溶剂,NH3与Cu2+的配位能力比H2O强,将H2O夺走,晶体的极性降低;
(4)根据晶胞密度计算公式ρ=![]() =
=![]() 计算。
计算。
(1)钛(Ti)的基态原子核外电子排布为1s22s22p63s23p63d24s2,M能层即为Ti核外第三层,M层中有3个能级,每个能级上的电子能量不同,则能量不同的电子有3种;
(2)①H2O、CH3OH、![]() 都是极性分子,根据钠与水和醇的反应剧烈程度可知,水中的氢活性较大更易电离,电离难易程度与极性关系,一般极性越大,越容易电离,则H2O中O-H键的极性大于CH3OH中O-H键的极性,水是中性的,苯酚具有酸性,说明苯酚中羟基上的H比水更易电离,则上述分子中O-H键的极性最强的是
都是极性分子,根据钠与水和醇的反应剧烈程度可知,水中的氢活性较大更易电离,电离难易程度与极性关系,一般极性越大,越容易电离,则H2O中O-H键的极性大于CH3OH中O-H键的极性,水是中性的,苯酚具有酸性,说明苯酚中羟基上的H比水更易电离,则上述分子中O-H键的极性最强的是![]() ;
;
②C、N、O位于同周期,同周期元素,随核电荷数增大,电负性逐渐增强,三种元素的电负性由大到小的顺序是O>N>C;
(3)配位键和单键都是σ键,根据图示,a为铜离子,b为NH3,c为H2O,铜离子与NH3、H2O形成6个配位键,每个NH3中含有3个σ键,每个H2O中含有两个σ键,则lmol该离子中所含σ键为1mol×(6+3×4+2×2)=22mol;根据相似相溶,乙醇为极性溶剂,H2O为极性分子,NH3与Cu2+的配位能力比H2O强,乙醇将H2O夺走,降低蓝色晶体的极性,则蓝色晶体的溶解度降低而析出;
(4)根据图2所示,金属铋原子位于六棱柱的顶点,面心和体心,该晶胞中铋原子的个数为2×![]() +3+
+3+![]() ×12=6个,根据图1所示,若铋原子的半径为rpm,则晶胞面的边长为2rpm,上下面的距离h=
×12=6个,根据图1所示,若铋原子的半径为rpm,则晶胞面的边长为2rpm,上下面的距离h=![]() rpm,将六棱柱看做6个三棱柱构成,每个三棱柱的体积为
rpm,将六棱柱看做6个三棱柱构成,每个三棱柱的体积为![]() ×2rpm×
×2rpm×![]() rpm×
rpm×![]() rpm=4
rpm=4![]() r3pm3=4
r3pm3=4![]() ×10-30r3cm3,则晶胞的体积为6×4
×10-30r3cm3,则晶胞的体积为6×4![]() ×10-30r3cm3=24
×10-30r3cm3=24![]() ×10-30r3cm3,则该晶胞的密度为ρ=
×10-30r3cm3,则该晶胞的密度为ρ=![]() =
=![]() =
=![]() =
= ![]() ×1030gcm-3。
×1030gcm-3。

【题目】室温下进行下列实验,根据实验操作和现象所得到的结论正确的是( )
选项 | 实验操作和现象 | 结 论 |
A | 将 | 生成了 |
B | 向浓度均为 |
|
C | 淀粉 | 还原性: |
D | 用pH试纸测得: |
|
A.AB.BC.CD.D
【题目】1,3-丁二烯是重要的化工原料,工业上常用1-丁烯催化脱氢的方法制备。将0.lmol1-丁烯和0.675mol水蒸气组成的混合气,在80kPa恒压下进行反应:CH3CH2CH=CH2(g)![]() CH2=CHCH=CH2(g)+H2(g)△H。
CH2=CHCH=CH2(g)+H2(g)△H。
请回答下列问题:
(1)已知化学键键能数据如下,由此计算△H=____________kJmo1-1。
化学键 | C-C | C=C | C-H | H-H |
键能/kJmol-1 | 348 | 612 | 412 | 436 |
(2)如图表示脱氢反应中温度对1-丁烯的平衡转化率的影响,工业生产通常控制反应温度600℃。
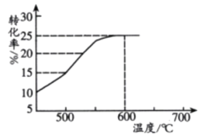
①请解释工业生产控制温度在600℃的原因___________。
②此温度下反应进行2.5h后达到平衡,从开始反应到建立平衡,以H2表示的反应速率为v(H2)=_________kPah-1;脱氢反应的平衡常数Kp=_________kPa(Kp为以分压表示的平衡常数,p分=p总×物质的量分数)。
(3)在密闭容器中反应达到平衡后,再充入1.575mol1-丁烯和1.625mol1,3-丁二烯,化学反应向_________(填“正反应”、“逆反应或“不移动”)方向进行 。