题目内容
4.下列说法正确的是:①Cl-的结构示意图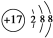 ②羟基的电子式:
②羟基的电子式: ;③HClO的结构式:H-Cl-O;④NaHCO3在水中的电离方程式:NaHCO3=Na++H++CO32-; ⑤Na2O的水溶液能导电,这不能说明Na2O是电解质; ⑥SiO2既能与氢氟酸反应又能与NaOH溶液反应,故SiO2是两性氧化物;⑦分馏、干馏、裂化都是化学变化( )
;③HClO的结构式:H-Cl-O;④NaHCO3在水中的电离方程式:NaHCO3=Na++H++CO32-; ⑤Na2O的水溶液能导电,这不能说明Na2O是电解质; ⑥SiO2既能与氢氟酸反应又能与NaOH溶液反应,故SiO2是两性氧化物;⑦分馏、干馏、裂化都是化学变化( )| A. | ①②⑤ | B. | ①④⑥⑦ | C. | ②③④⑥ | D. | ②③⑤⑥⑦ |
分析 ①Cl-的质子数为17,核外电子为18;
②羟基为-OH,O原子的周围有7个电子;
③HClO中O可形成2个共价键;
④NaHCO3在水中的电离出Na+、HCO3-;
⑤Na2O熔融状态下能导电,Na2O是电解质;
⑥SiO2既能与氢氟酸反应又能与NaOH溶液反应,但SiO2是酸性氧化物;
⑦干馏、裂化都是化学变化,分馏为物理变化.
解答 解:①Cl-的质子数为17,核外电子为18,则Cl-的结构示意图为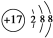 ,故正确;
,故正确;
②羟基为-OH,O原子的周围有7个电子,则羟基的电子式为 ,故正确;
,故正确;
③HClO中O可形成2个共价键,结构式为H-O-Cl,故错误;
④NaHCO3在水中的电离出Na+、HCO3-,电离方程式为NaHCO3=Na++HCO3-,故错误;
⑤Na2O熔融状态下能导电,Na2O是电解质,而Na2O的水溶液能导电,NaOH发生电离,故正确;
⑥SiO2既能与氢氟酸反应又能与NaOH溶液反应,但SiO2是酸性氧化物,与HF酸反应为特性,故错误;
⑦干馏生成煤焦油等、裂化生成小分子烃等,均有新物质生成,都是化学变化,而分馏与混合物的沸点有关,为物理变化,故错误;
故选.
点评 本题考查化学用语,为高频考点,把握结构示意图、电子式、结构式、电离方程式等为解答的关键,侧重分析与应用能力的考查,注意酸性氧化物的判断,题目难度不大.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
14.下列有关海水综合利用的说法正确的是( )
| A. | 从海水中可以得到NaCl,电解熔融NaCl可获得Cl2 | |
| B. | 海水中含有钾元素,只需经过物理变化就可以得到钾单质 | |
| C. | 海水蒸发制海盐的过程只发生了化学变化 | |
| D. | 利用电解的方法可以从海水中获取淡水 |
12.下列各种物质在一定条件下反应,所得产物种类与反应物的用量或条件无关的是( )
①Fe+O2
②Na2SiO3+CO2+H2O
③NH4HCO3+NaOH
④Cu+Cl2
⑤Ca(HCO3)2+Ca(OH)2.
①Fe+O2
②Na2SiO3+CO2+H2O
③NH4HCO3+NaOH
④Cu+Cl2
⑤Ca(HCO3)2+Ca(OH)2.
| A. | ④⑤ | B. | ②③ | C. | ①⑤ | D. | ①②⑤ |
19.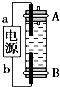 某同学设计了一种利用电解法制取Fe(OH)2的实验装置(如图),通电后,溶液中产生白色沉淀,且较长时间不变色.下列说法中正确的是( )
某同学设计了一种利用电解法制取Fe(OH)2的实验装置(如图),通电后,溶液中产生白色沉淀,且较长时间不变色.下列说法中正确的是( )
 某同学设计了一种利用电解法制取Fe(OH)2的实验装置(如图),通电后,溶液中产生白色沉淀,且较长时间不变色.下列说法中正确的是( )
某同学设计了一种利用电解法制取Fe(OH)2的实验装置(如图),通电后,溶液中产生白色沉淀,且较长时间不变色.下列说法中正确的是( )| A. | 电源中a一定为负极,b一定为正极 | |
| B. | 可以用NaCl作为电解质,但不能用Na2SO4 | |
| C. | A、B两端都必须用铁作电极 | |
| D. | 阴极上发生的反应是:2H++2e-═H2↑ |
9.下列变化中,属于物理变化的是( )
| A. | 煤的干馏 | B. | 石油的分馏 | C. | 石蜡油的裂化 | D. | 铝热反应 |
13.铝能用于冶炼一些金属(如:钒、铬、锰等),这是因为铝( )
| A. | 具有较强的还原性 | B. | 既能与酸反应,又能与碱反应 | ||
| C. | 熔点低 | D. | 导电性好 |
14.下列合成高分子化合物的化学方程式中,错误的是不考虑反应条件( )
| A. | nCH2=CHCH2COOH→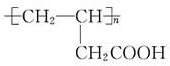 | |
| B. | nHOOC(CH2)5OH?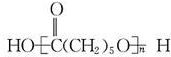 +(n-1)H2O +(n-1)H2O | |
| C. | n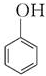 +nHCHO$\stackrel{H+}{→}$ +nHCHO$\stackrel{H+}{→}$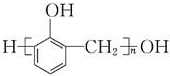 +(2n-1)H2O +(2n-1)H2O | |
| D. | nHOOC(CH2)4COOH+nHO(CH2)2OH?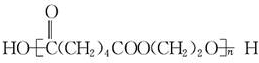 +(2n-1)H2O +(2n-1)H2O |