题目内容
19.Al单质的晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示.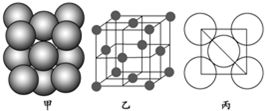
若已知Al的原子半径为d pm,NA代表阿伏加德罗常数,Al的相对原子质量27.通过计算确定:
(1)一个晶胞中Al原子的数目.
(2)Al晶胞的密度表达式.
分析 (1)可以均摊法计算晶胞中Al原子数目;
(2)结合Al的摩尔质量计算晶胞质量,Al的原子半径为d pm,则晶胞棱长为4d pm×$\frac{\sqrt{2}}{2}$=2$\sqrt{2}$d pm,再根据ρ=$\frac{m}{V}$计算晶胞密度.
解答 解:(1)晶胞中Al原子数目为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,
答:一个晶胞中Al原子的数目为4;
(2)晶胞质量为4×$\frac{27}{{N}_{A}}$g,Al的原子半径为d pm,则晶胞棱长为4d pm×$\frac{\sqrt{2}}{2}$=2$\sqrt{2}$d pm,故Al晶胞的密度ρ=$\frac{m}{V}$=$\frac{4×\frac{27}{{N}_{A}}}{(2\sqrt{2}d×1{0}^{-10}cm)^{3}}$=$\frac{27}{4\sqrt{2}(d×1{0}^{-10})^{3}{N}_{A}}$=g.cm-3,
答:Al晶胞的密度为=$\frac{27}{4\sqrt{2}(d×1{0}^{-10})^{3}{N}_{A}}$g.cm-3.
点评 本题考查晶胞计算,注意利用均摊法计算晶胞质量,需要学生具有一定的数学计算能力,难度中等.

练习册系列答案
相关题目
7.下列有关平衡常数K的说法中正确的是( )
| A. | 平衡常数与反应物或生成物的浓度变化无关,温度越高,平衡常数越大 | |
| B. | 25℃时,Mg(OH)2固体在同体积、同浓度的氨水和NH4Cl溶液中的Ksp相比较,前者较小 | |
| C. | 25℃时NH4Cl溶液中的Kw大于100℃时NaCl溶液中的Kw | |
| D. | 2S℃时,H2SO3溶液的一级电离常数为Ka,则NaHSO3溶液的水解常数Kb=$\frac{Kw}{Ka}$ |
11.向盛有0.1mol/L AgNO3溶液的试管中,滴加0.1mol/L Na2S溶液直至沉淀完全,再向其中滴加足量NaCl溶液,产生的现象或生成的物质是( )
已知:Ksp(AgCl)=1.8×10-10;Ksp(Ag2S)=6.3×10-50.
已知:Ksp(AgCl)=1.8×10-10;Ksp(Ag2S)=6.3×10-50.
| A. | 黑色沉淀完全转化为白色沉淀 | B. | 既有氯化银也有硫化银 | ||
| C. | 不能由黑色沉淀转化为白色沉淀 | D. | 只有氯化银白色沉淀 |