题目内容
黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可制备硫和铁的化合物.
(1)冶炼铜的反应为:8CuFeS2+21O2
8Cu+4FeO+2Fe2O3+16SO2
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是 (填元素符号).
(2)上述冶炼过程产生大量SO2.下列处理方案中合理的是 (填代号).
a.高空排放 b.用于制备硫酸 c.用纯碱溶液吸收制Na2SO3d.用浓硫酸吸收
(3)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3.方法为:
①用稀盐酸浸取炉渣、过滤.
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3.
根据以上信息回答下列问题:
a.除去Al3+的离子方程式是 .
b.选用提供的试剂,设计实验验证炉渣中含有FeO.
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 KMnO4溶液 NaOH溶液 碘水
所选试剂为 .证明炉渣中含有FeO的实验现象为 .
(1)冶炼铜的反应为:8CuFeS2+21O2
| ||
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是
(2)上述冶炼过程产生大量SO2.下列处理方案中合理的是
a.高空排放 b.用于制备硫酸 c.用纯碱溶液吸收制Na2SO3d.用浓硫酸吸收
(3)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3.方法为:
①用稀盐酸浸取炉渣、过滤.
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3.
根据以上信息回答下列问题:
a.除去Al3+的离子方程式是
b.选用提供的试剂,设计实验验证炉渣中含有FeO.
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 KMnO4溶液 NaOH溶液 碘水
所选试剂为
考点:铜金属及其重要化合物的主要性质,制备实验方案的设计
专题:实验设计题,元素及其化合物
分析:(1)反应中化合价降低的元素被还原;
(2)冶炼过程产生大量SO2,处理方案中合理的分析是二氧化硫是污染性气体,不能排放到空气中,可以吸收利用;
(3)a、氧化铝是两性氧化物,能和强酸以及强碱反应,利用氢氧化钠使其变为偏铝酸根即可;
b、亚铁离子能被高锰酸钾溶液氧化,使的高锰酸钾溶液褪色.
(2)冶炼过程产生大量SO2,处理方案中合理的分析是二氧化硫是污染性气体,不能排放到空气中,可以吸收利用;
(3)a、氧化铝是两性氧化物,能和强酸以及强碱反应,利用氢氧化钠使其变为偏铝酸根即可;
b、亚铁离子能被高锰酸钾溶液氧化,使的高锰酸钾溶液褪色.
解答:
解:(1)化合价降低的元素Cu、O,在反应中被还原,故答案为:Cu、O;
(2)冶炼过程产生大量SO2.分析下列处理方案:
a.二氧化硫是污染性气体,高空排放会污染空气,处理不合理,故a错误;
b.可以利用吸收二氧化硫生成硫酸,用于制备硫酸,故b合理;
c.用纯碱溶液吸收二氧化硫可以制Na2SO4,故c合理;
d.用浓硫酸不能吸收二氧化硫,故d不合理;
故答案为:b、c.
(3)a.氧化铝是两性氧化物,能和强酸以及强碱反应,6H++Al2O3=3H2O+2Al3+,除去铝离子的反应是利用过量氢氧化钠溶液和铝离子反应生成偏铝酸根,
故答案为:Al3++4OH-=2H2O+AlO2-;
b.高锰酸钾溶液能氧化亚铁离子,使得高锰酸钾溶液褪色,故答案为:稀硫酸、KMnO4溶液;稀硫酸浸取炉渣所得溶液使KMnO4溶液褪色.
(2)冶炼过程产生大量SO2.分析下列处理方案:
a.二氧化硫是污染性气体,高空排放会污染空气,处理不合理,故a错误;
b.可以利用吸收二氧化硫生成硫酸,用于制备硫酸,故b合理;
c.用纯碱溶液吸收二氧化硫可以制Na2SO4,故c合理;
d.用浓硫酸不能吸收二氧化硫,故d不合理;
故答案为:b、c.
(3)a.氧化铝是两性氧化物,能和强酸以及强碱反应,6H++Al2O3=3H2O+2Al3+,除去铝离子的反应是利用过量氢氧化钠溶液和铝离子反应生成偏铝酸根,
故答案为:Al3++4OH-=2H2O+AlO2-;
b.高锰酸钾溶液能氧化亚铁离子,使得高锰酸钾溶液褪色,故答案为:稀硫酸、KMnO4溶液;稀硫酸浸取炉渣所得溶液使KMnO4溶液褪色.
点评:本题是对金属的化学性质的考查,要求学生熟记教材知识,学以致用,综合性较强,难度中等.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
下列溶液中的氯离子浓度与50mL 0.5mol?L-1的AlCl3溶液中氯离子浓度相等的是( )
| A、150 mL 1 mol?L-1的KClO3 |
| B、75 mL 1.5 mol?L-1的NH4Cl |
| C、75 mL 2 mol?L-1的CaCl2 |
| D、150 mL 3 mol?L-1的KCl |

 如图所示为电解水的装置,闭合开关S后,观察到电压表示数为6.0V,电流表示数为100mA.
如图所示为电解水的装置,闭合开关S后,观察到电压表示数为6.0V,电流表示数为100mA.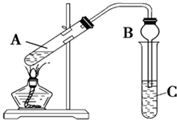 某兴趣小组利用如图装置,将不同浓度的硫酸与3mL 无水乙醇和2mL冰醋酸混合,分别进行制取乙酸乙酯的研究.
某兴趣小组利用如图装置,将不同浓度的硫酸与3mL 无水乙醇和2mL冰醋酸混合,分别进行制取乙酸乙酯的研究.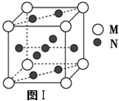 ,则该合金中M和N的原子个数比为
,则该合金中M和N的原子个数比为 ,其中M离子的配位数是
,其中M离子的配位数是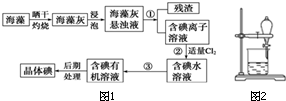 海洋植物如海带、海藻中含有大量的碘元素,碘元素以碘离子的形式存在.实验室里从海藻中提取碘的流程如图1:
海洋植物如海带、海藻中含有大量的碘元素,碘元素以碘离子的形式存在.实验室里从海藻中提取碘的流程如图1: