题目内容
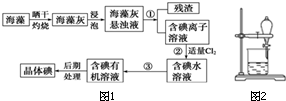 海洋植物如海带、海藻中含有大量的碘元素,碘元素以碘离子的形式存在.实验室里从海藻中提取碘的流程如图1:
海洋植物如海带、海藻中含有大量的碘元素,碘元素以碘离子的形式存在.实验室里从海藻中提取碘的流程如图1:(1)实验室焙烧海带,需要下列仪器中的
a.试管 b.烧杯c.坩埚 d.泥三角e.铁三脚架 f.酒精灯
(2)指出提取碘的过程中有关的实验操作名称:①
(3)提取碘的过程中,可选择的有机试剂是
A.甲苯、酒精
B.四氯化碳、苯
C.汽油、乙酸
D.汽油、甘油
(4)③过程需要使用的主要玻璃仪器为
(5)某小组用CCl4萃取碘水中的碘,在如图2的分液漏斗中,下层液体呈
(6)从含碘的有机溶液中提取碘和回收有机溶剂,所用的分离方法为
考点:海水资源及其综合利用
专题:实验设计题
分析:(1)灼烧海带需要的仪器有:酒精灯、三脚架、泥三角及坩埚;
(2)分离难溶性固体和溶液采用过滤方法,从碘水中分离出碘采用分液方法;
(3)萃取剂的选取标准:和原溶剂不互溶,和溶质不反应,溶质在萃取剂中的溶解度大于在水中的溶解度;
(4)③的操作是萃取,需要分液漏斗和烧杯;
(5)四氯化碳的密度大于水且和水不互溶,四氯化碳能萃取碘,所以有机层在下方、水在上方;如果分液漏斗上口活塞小孔未与空气相通,则液体不会流出;
(6)从含碘的有机溶液中提取碘和回收有机溶剂,利用物质的沸点不同,利用蒸馏的方法进行分离;
(2)分离难溶性固体和溶液采用过滤方法,从碘水中分离出碘采用分液方法;
(3)萃取剂的选取标准:和原溶剂不互溶,和溶质不反应,溶质在萃取剂中的溶解度大于在水中的溶解度;
(4)③的操作是萃取,需要分液漏斗和烧杯;
(5)四氯化碳的密度大于水且和水不互溶,四氯化碳能萃取碘,所以有机层在下方、水在上方;如果分液漏斗上口活塞小孔未与空气相通,则液体不会流出;
(6)从含碘的有机溶液中提取碘和回收有机溶剂,利用物质的沸点不同,利用蒸馏的方法进行分离;
解答:
解:(1)灼烧海带需要的仪器有:酒精灯、三脚架、泥三角及坩埚,故选cdef;
(2)分离难溶性固体和溶液采用过滤方法,从碘水中分离出碘采用分液方法,所以①的操作名称是过滤,③的操作名称是分液,故答案为:过滤;分液;
(3)A.酒精和水互溶,所以不能作萃取剂,故错误;
B.四氯化碳、苯符合萃取剂条件,所以能作萃取剂,故B正确;
C.汽油和碘反应,乙酸和水互溶,所以汽油、乙酸不能作萃取剂,故错误;
D.汽油和碘反应、甘油和水互溶,所以汽油、甘油不能作萃取剂,故错误;
故选B;
(4)③的操作是萃取,需要分液漏斗和烧杯,故答案为:分液漏斗和烧杯;
(5)四氯化碳的密度大于水且和水不互溶,四氯化碳能萃取碘,所以有机层在下方、水在上方,碘的四氯化碳溶液呈紫色;如果分液漏斗上口活塞小孔未与空气相通,则液体不会流出;
故答案为:紫红色;分液漏斗上口活塞小孔未与空气相通;
(6)从含碘的有机溶液中提取碘和回收有机溶剂,利用物质的沸点不同,利用蒸馏的方法进行分离;
故答案为:蒸馏;
(2)分离难溶性固体和溶液采用过滤方法,从碘水中分离出碘采用分液方法,所以①的操作名称是过滤,③的操作名称是分液,故答案为:过滤;分液;
(3)A.酒精和水互溶,所以不能作萃取剂,故错误;
B.四氯化碳、苯符合萃取剂条件,所以能作萃取剂,故B正确;
C.汽油和碘反应,乙酸和水互溶,所以汽油、乙酸不能作萃取剂,故错误;
D.汽油和碘反应、甘油和水互溶,所以汽油、甘油不能作萃取剂,故错误;
故选B;
(4)③的操作是萃取,需要分液漏斗和烧杯,故答案为:分液漏斗和烧杯;
(5)四氯化碳的密度大于水且和水不互溶,四氯化碳能萃取碘,所以有机层在下方、水在上方,碘的四氯化碳溶液呈紫色;如果分液漏斗上口活塞小孔未与空气相通,则液体不会流出;
故答案为:紫红色;分液漏斗上口活塞小孔未与空气相通;
(6)从含碘的有机溶液中提取碘和回收有机溶剂,利用物质的沸点不同,利用蒸馏的方法进行分离;
故答案为:蒸馏;
点评:本题考查海水资源综合利用,侧重考查学生对化学实验基本操作能力的掌握,明确实验原理是解本题关键,知道萃取剂的选取标准,知道常见仪器作用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
实验室加热氯酸钾与MnO2的混合物制氧气,从剩余物中回收二氧化锰的操作顺序正确的是( )
| A、溶解、过滤、蒸发、洗涤 |
| B、溶解、过滤、洗涤、干燥 |
| C、溶解、蒸发、洗涤、过滤 |
| D、溶解、洗涤、过滤、干燥 |
下列转化不能一步实现的是( )
| A、CuO→Cu(OH)2 |
| B、CuSO4→Cu |
| C、CaCO3→CaO |
| D、MgSO4→MgCl2 |
把0.02mol?L-1 CH3COOH溶液和0.01mol?L-1 NaOH溶液以等体积混合,混合溶液中粒子浓度关系正确的是( )
| A、c(CH3COO-)>c(Na+) |
| B、c(CH3COOH)>c(CH3COO-) |
| C、c(H+)<c(OH-) |
| D、c(CH3COO-)>+c(CH3COOH)=0.02mol?L-1 |
某工厂的废渣中混有少量的锌粉和氧化铜(其它成分不跟酸反应),跟废盐酸接触形成污水.若向该污水中撒入铁粉,反应后铁粉有剩余,所得溶液中一定含有的金属离子是( )
| A、Fe2+、Cu2+ |
| B、Cu2+、Zn2+ |
| C、Zn2+、Fe2+ |
| D、Zn2+、Fe3+ |