题目内容
配平下列化学方程式: Zn+ HNO3═ Zn(NO3)2+ N2O↑+ H2O,产生11.2L N2O气体(标准状况下)转移 个电子.
考点:氧化还原反应方程式的配平
专题:氧化还原反应专题
分析:在该反应中,Zn元素化合价升高,N元素化合价降低,反应中氧化剂为HNO3,还原剂为Zn,N2O为还原产物,Zn(NO3)2为氧化产物,硝酸既表现氧化性又表现酸性,所以应根据化合价升降想等配平氧化剂和还原剂,然后根据原子守恒配平整个方程式.
解答:
解:在该反应中,Zn元素化合价升高,N元素化合价降低,反应中氧化剂为HNO3,还原剂为Zn,N2O为还原产物,Zn(NO3)2为氧化产物,
Zn→Zn(NO3)2,Zn的化合价0→+2,升高2,
HNO3→N2O,N的化合价由+5→+1,降低4,生成一个N2O,N的化合价降低4×2=8,
根据化合价升降相等可知,Zn(NO3)2的化学计量数4,N2O的化学计量数为1,
根据原子守恒配平得:4Zn+10HNO3=4Zn(NO3)2+N2O↑+5H2O,
n(N2O)=
=0.5mol,生成一个N2O,N的化合价降低4×2=8,即生成一个N2O转移电子数为8,
生成0.5molN2O时,转移电子的物质的量为0.5mol×8=4mol,因此转移电子数为4mol×NAmol-1=4NA,
故答案为:4;10;4;1;5;4NA.
Zn→Zn(NO3)2,Zn的化合价0→+2,升高2,
HNO3→N2O,N的化合价由+5→+1,降低4,生成一个N2O,N的化合价降低4×2=8,
根据化合价升降相等可知,Zn(NO3)2的化学计量数4,N2O的化学计量数为1,
根据原子守恒配平得:4Zn+10HNO3=4Zn(NO3)2+N2O↑+5H2O,
n(N2O)=
| 11.2L |
| 22.4L/mol |
生成0.5molN2O时,转移电子的物质的量为0.5mol×8=4mol,因此转移电子数为4mol×NAmol-1=4NA,
故答案为:4;10;4;1;5;4NA.
点评:本题考查了氧化还原反应的配平和转移电子数的计算,难度中等,注意此反应中硝酸既表现氧化性又表现酸性,因此不能先配平氧化剂和还原剂,应先配平氧化产物和还原产物.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
如图是某厂采用电解法处理石油炼制过程中产生的大量H2S废气的工艺流程.该方法对H2S的吸收率达99%以上,并可制取H2和S.下列说法正确的是( )

| A、可采取在足量空气中充分燃烧的方法消除H2S的污染 |
| B、反应②中的阴极反应式为2H++2e-═H2↑,电解后所得溶液呈酸性 |
| C、如反应①中H2S过量,则反应离子方程式为:2Fe3++3H2S═2FeS↓+S↓+6H+ |
| D、此反应流程图中可循环利用的物质是FeCl3溶液,FeCl3可用作杀菌、消毒剂和净水剂 |
把0.02mol?L-1 CH3COOH溶液和0.01mol?L-1 NaOH溶液以等体积混合,混合溶液中粒子浓度关系正确的是( )
| A、c(CH3COO-)>c(Na+) |
| B、c(CH3COOH)>c(CH3COO-) |
| C、c(H+)<c(OH-) |
| D、c(CH3COO-)>+c(CH3COOH)=0.02mol?L-1 |
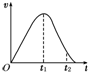 把除去氧化膜的镁条放入盛有一定浓度的稀盐酸的试管中,发现H2的生成速率v随时间t的变化关系如图所示.其中O~t1段速率变化的主要因素是
把除去氧化膜的镁条放入盛有一定浓度的稀盐酸的试管中,发现H2的生成速率v随时间t的变化关系如图所示.其中O~t1段速率变化的主要因素是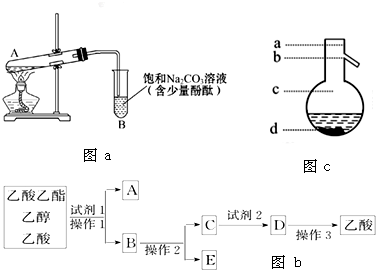
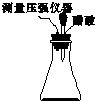 某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和炭粉置于锥形瓶底部,塞上瓶塞(如图所示).从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化.
某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和炭粉置于锥形瓶底部,塞上瓶塞(如图所示).从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化.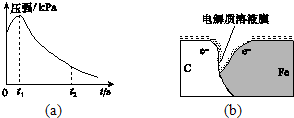 (3)该小组对图(a)中0~t1时压强变大的原因提出了如下假设,请你完成假设二:
(3)该小组对图(a)中0~t1时压强变大的原因提出了如下假设,请你完成假设二: