题目内容
(1)把少量的金属钠分别放入钠放入FeCl3溶液中,现象是 ,离子方程式是 .
(2)在铝质易拉罐中收集满CO2气体,然后在其中倒入10mL浓NaOH溶液,并迅速用胶带将易拉罐口封住,能够观察到的实验现象是易拉罐突然变瘪了,可经过一段时间之后,又可以观察到的现象是 .试解释易拉罐变瘪的原因 ;并解释后一现象的原因 .写出反应过程中的两个离子方程式 .
(2)在铝质易拉罐中收集满CO2气体,然后在其中倒入10mL浓NaOH溶液,并迅速用胶带将易拉罐口封住,能够观察到的实验现象是易拉罐突然变瘪了,可经过一段时间之后,又可以观察到的现象是
考点:钠的化学性质,铝的化学性质
专题:
分析:(1)钠的密度小于水,熔点较低,且钠和水剧烈反应生成氢氧化钠和氢气,氢氧化钠和氯化铁反应生成氢氧化铁红褐色沉淀;
(2)在铝质易拉罐中收集满CO2气体,然后在其中倒入10mL浓NaOH溶液,并迅速用胶带将易拉罐口封住,易拉罐中的NaOH与CO2反应,使得易拉罐内压强变小,内外产生了压强差,易拉罐被大气压压瘪了,CO2+2OH-=CO32-+H2O;
过量的NaOH可与铝反应生成氢气,使得易拉罐内压强变大,易拉罐又会鼓起来,2Al+2NaOH+2H2O=2NaAlO2+3H2↑;据此分析即可解答.
(2)在铝质易拉罐中收集满CO2气体,然后在其中倒入10mL浓NaOH溶液,并迅速用胶带将易拉罐口封住,易拉罐中的NaOH与CO2反应,使得易拉罐内压强变小,内外产生了压强差,易拉罐被大气压压瘪了,CO2+2OH-=CO32-+H2O;
过量的NaOH可与铝反应生成氢气,使得易拉罐内压强变大,易拉罐又会鼓起来,2Al+2NaOH+2H2O=2NaAlO2+3H2↑;据此分析即可解答.
解答:
解:(1)钠的密度小于水,所以钠会浮在水面上,钠的熔点较低,钠和水反应放出大量的热,而使钠熔成小球,钠和水反应放出的氢气使钠受力不均,导致钠四处游动,且放出嘶嘶的声音,钠和水反应生成氢氧化钠,氢氧化钠和氯化铁溶液反应生成红褐色沉淀氢氧化铁,所以看到的现象是:钠熔化成小球四处游动并发出嘶嘶的声音,有气泡产生,有红褐色沉淀生成;
反应方程式为:2Na+2H2O=2Na++2OH-+H2↑、Fe3++3OH-=Fe(OH)3↓;
故答案为:钠熔化成小球四处游动并发出嘶嘶的声音,有气泡产生,有红褐色沉淀生成;2Na+2H2O=2Na++2OH-+H2↑、Fe3++3OH-=Fe(OH)3↓;
(2)在铝质易拉罐中收集满CO2气体,然后在其中倒入10mL浓NaOH溶液,并迅速用胶带将易拉罐口封住,易拉罐突然变瘪了,这是因为易拉罐中的CO2与浓NaOH反应,CO2+2NaOH═Na2CO3+H2O,其反应的离子方程式是 CO2+2OH-=CO32-+H2O;二氧化碳气体被氢氧化钠吸收,使得易拉罐内压强变小,内外产生了压强差,易拉罐被大气压压瘪;
可经过一段时间之后,又可以观察到的现象是易拉罐又鼓起来了,是因为浓NaOH与易拉罐(Al)反应产生H2,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,其反应的离子方程式是2Al+2OH-+2H2O=2AlO2-+3H2↑,随着易拉罐内H2量的增多,易拉罐内气压增大,易拉罐又鼓起来了;
故答案为:易拉罐又鼓起来;易拉罐中的CO2与浓NaOH反应,致使易拉罐内气压降低,从而使易拉罐被大气压压瘪;浓NaOH与易拉罐(Al)反应产生H2,随着易拉罐内H2量的增多,易拉罐内气压增大;CO2+2OH-=CO32-+H2O;2Al+2OH-+2H2O=2AlO2-+3H2↑.
反应方程式为:2Na+2H2O=2Na++2OH-+H2↑、Fe3++3OH-=Fe(OH)3↓;
故答案为:钠熔化成小球四处游动并发出嘶嘶的声音,有气泡产生,有红褐色沉淀生成;2Na+2H2O=2Na++2OH-+H2↑、Fe3++3OH-=Fe(OH)3↓;
(2)在铝质易拉罐中收集满CO2气体,然后在其中倒入10mL浓NaOH溶液,并迅速用胶带将易拉罐口封住,易拉罐突然变瘪了,这是因为易拉罐中的CO2与浓NaOH反应,CO2+2NaOH═Na2CO3+H2O,其反应的离子方程式是 CO2+2OH-=CO32-+H2O;二氧化碳气体被氢氧化钠吸收,使得易拉罐内压强变小,内外产生了压强差,易拉罐被大气压压瘪;
可经过一段时间之后,又可以观察到的现象是易拉罐又鼓起来了,是因为浓NaOH与易拉罐(Al)反应产生H2,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,其反应的离子方程式是2Al+2OH-+2H2O=2AlO2-+3H2↑,随着易拉罐内H2量的增多,易拉罐内气压增大,易拉罐又鼓起来了;
故答案为:易拉罐又鼓起来;易拉罐中的CO2与浓NaOH反应,致使易拉罐内气压降低,从而使易拉罐被大气压压瘪;浓NaOH与易拉罐(Al)反应产生H2,随着易拉罐内H2量的增多,易拉罐内气压增大;CO2+2OH-=CO32-+H2O;2Al+2OH-+2H2O=2AlO2-+3H2↑.
点评:本题主要考查了钠和铝的化学性质,正确分析钠与盐溶液反应的过程和铝能与氢氧化钠反应这一化学性质与易拉罐压强变化的关系是解答的关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
一定质量的A1、Mg合金与适量的稀硫酸恰好完全反应,将反应后的溶液蒸干,所得固体(不含结晶水)质量比原固体增加了4.8g,则该合金的物质的量可能为( )
| A、0.04mol |
| B、0.05mol |
| C、0.06mol |
| D、0.07mol |
常温下0.1mol/L某一元酸(HA)溶液中
=10-8,下列叙述正确的是( )
| c(OH-) |
| c(H+) |
| A、溶液中水电离出的c(H+)=10-10mol/L |
| B、溶液中c(HA)+c(A-)=0.1mol/L |
| C、与0.05mol/LNaOH溶液等体积混合所得溶液中离子浓度大小关系为c(H+)<c(OH-)<c(Na+)<c(A-) |
| D、上述溶液中加入一定量CH3COONa晶体或加水稀释,溶液的c(OH-)减小 |
甲烷分子是以碳原子为中心的正四面体形结构,而不是正方形的平面结构,理由是( )
| A、CH3Cl只有一种空间结构 |
| B、CH2Cl2只有一种空间结构 |
| C、CHCl3只有一种空间结构 |
| D、CCl4是非极性分子 |
在某温度下测得纯水中的c(H+)=2.4×10-7mol?L-1,则c(OH-)为( )
| A、2.4×10-7mol?L-1 | ||
| B、0.14×10-7mol?L-1 | ||
C、
| ||
| D、无法确定 |
联合国气候变化大会将于12月7日在丹麦哥本哈根召开,这次大会旨在达成一个真正全球性的、目标远大的(温室气体)减排协议.下列与此相关的叙述中,正确的是( )
| A、化学面对现代日益严重的环境问题显得越来越无能为力了 |
| B、化学是“污染”的代名词,一切污染皆因化学而起 |
| C、化学及分支学科面临着罕见的窘境,被人们淡忘、不重视是合乎情理的 |
| D、能源和环境问题的解决,过去、现在和将来都有赖于化学学科的发展 |
关于下列四个图象的说法正确的是( )


| A、图①表示H2与O2发生反应过程中的能量变化,H2的燃烧热为241.8kJ?mol-1 |
| B、图②是在电解氯化钠稀溶液的电解池中,阴、阳极产生气体体积之比一定为1:1 |
| C、图③表示常温下稀释 HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB溶液 |
| D、图④表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(g) 的影响,乙的压强大 |
氧化性随原子序数的增加而增强的是( )
| A、F-、Cl-、Br- |
| B、Na+、Mg2+、Al3+ |
| C、P、S、Cl |
| D、Li+、Na+、K+ |
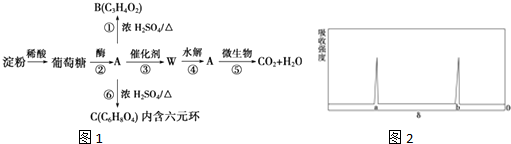
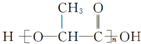 ,有关W的信息如图,据此回答下列问题:
,有关W的信息如图,据此回答下列问题: