题目内容
一定质量的A1、Mg合金与适量的稀硫酸恰好完全反应,将反应后的溶液蒸干,所得固体(不含结晶水)质量比原固体增加了4.8g,则该合金的物质的量可能为( )
| A、0.04mol |
| B、0.05mol |
| C、0.06mol |
| D、0.07mol |
考点:有关混合物反应的计算
专题:计算题
分析:铝和镁与稀硫酸反应生成硫酸铝、硫酸镁,蒸干后得到硫酸铝、硫酸镁,固体质量增加的部分为硫酸根离子的质量,根据n=
可计算出硫酸根离子的物质的量,然后根据硫酸铝、硫酸镁的化学式通过讨论得出合金物质的量的范围.
| m |
| M |
解答:
解:反应后溶液蒸干为硫酸铝、硫酸镁,硫酸铝、硫酸镁的总质量比原固体增加了4.8g,所以增重为硫酸根的质量,硫酸根离子物质的量为:
=0.05mol,
若只有硫酸镁,金属的物质的量最多,n(Mg)=n(MgSO4)=0.05mol,
若只有硫酸铝金属的物质的量最少,n(Al)=
×n[Al2(SO4)3]=
×005mol=0.03mol,
故金属的物质的量介于0.03mol~0.05mol之间.
只有选项A正确,
故选A.
| 4.8g |
| 96g/mol |
若只有硫酸镁,金属的物质的量最多,n(Mg)=n(MgSO4)=0.05mol,
若只有硫酸铝金属的物质的量最少,n(Al)=
| 2 |
| 3 |
| 2 |
| 3 |
故金属的物质的量介于0.03mol~0.05mol之间.
只有选项A正确,
故选A.
点评:本题考查了有关混合物反应的计算,题目难度中等,明确增重的4.8g为硫酸根离子的质量为解答关键,试题有利于培养学生的分析、理解能力及化学计算能力.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
下列各组离子,在溶液中能大量共存,并且溶液呈无色的是( )
| A、K+、Al3+、NO3-、AlO2- |
| B、K+、H+、MnO4-、SO42- |
| C、Ba2+、Cl-、Na+、OH- |
| D、Fe2+、H+、SO42-、NO3- |
常温下,有关pH=3的醋酸溶液的说法正确的是( )
| A、醋酸溶液中,水的电离平衡向右移动 |
| B、加水稀释100倍后,溶液的pH=5 |
| C、加入CH3COONa固体,水的离子积常数Kw变小 |
| D、加入冰醋酸,醋酸的电离程度变小 |
下列离子方程式书写正确的是( )
A、用铂电极电解氯化镁溶液:Cl-+2H2O
| ||||
| B、NaHSO4溶液中滴人Ba(OH)2溶液至中性:H++SO42-+Ba2+十OH-═BaSO4↓+H2O | ||||
| C、在H2O2中加入酸性KMnO4溶液:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O | ||||
| D、稀HNO3中加入过量的Fe粉:Fe十4H+十NO3-═Fe3++NO↑+2H2O |
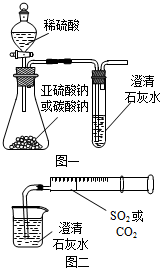 某同学用如图一所示的装置来探究CO2、SO2与澄清石灰水的反应,结果通入CO2可以看到先浑浊后澄清的现象,但通入SO2没有能看到浑浊现象.经过思考分析后,该同学改用图二的装置,将气体收集在注射器,缓慢地将气体一个气泡一个气泡地通入澄清石灰水中,都能看到石灰水先变浑浊再澄清的现象,且通入SO2产生现象明显比通入CO2快.
某同学用如图一所示的装置来探究CO2、SO2与澄清石灰水的反应,结果通入CO2可以看到先浑浊后澄清的现象,但通入SO2没有能看到浑浊现象.经过思考分析后,该同学改用图二的装置,将气体收集在注射器,缓慢地将气体一个气泡一个气泡地通入澄清石灰水中,都能看到石灰水先变浑浊再澄清的现象,且通入SO2产生现象明显比通入CO2快.