题目内容
下列事实不能用勒夏特列原理解释的是( )
| A、工业制取金属钾:Na(l)+KCl(l)?NaCl(l)+K(g),选取适宜的温度,使K成蒸汽从反应混合物中分离出来 |
| B、开启啤酒瓶时,有大量泡沫状气泡涌出瓶口 |
| C、工业合成氨气,采用铁触媒,并在500℃进行反应 |
| D、对于2HI(g)?H2(g)+I2(g);△H>0,升高温度可使颜色变深 |
考点:化学平衡移动原理
专题:化学平衡专题
分析:勒夏特列原理为:如果改变影响平衡的条件之一,平衡将向着能够减弱这种改变的方向移动.使用勒夏特列原理时,该反应必须是可逆反应,否则勒夏特列原理不适用.
解答:
解:A、Na(l)+KCl(l)?NaCl(l)+K(g),使K成蒸汽从反应混合物中分离出来,即减小产物的浓度,能让平衡向着正方向进行,能用勒夏特列原理解释,故A错误;
B、开启啤酒瓶后,瓶中马上泛起大量泡沫,是压强对其影响导致的,属于可逆反应,能用勒夏特列原理解释,故B错误;
C、业合成氨气,采用铁触媒,并在500℃进行反应,是为了保证催化剂的催化活性高,化学反应速率加快,不能用勒夏特列原理解释,故C正确;
D、对于2HI(g)?H2(g)+I2(g);△H>0,升高温度,平衡正向移动,碘蒸汽浓度增大,使颜色变深,能用勒夏特列原理解释,故D错误.
故选C.
B、开启啤酒瓶后,瓶中马上泛起大量泡沫,是压强对其影响导致的,属于可逆反应,能用勒夏特列原理解释,故B错误;
C、业合成氨气,采用铁触媒,并在500℃进行反应,是为了保证催化剂的催化活性高,化学反应速率加快,不能用勒夏特列原理解释,故C正确;
D、对于2HI(g)?H2(g)+I2(g);△H>0,升高温度,平衡正向移动,碘蒸汽浓度增大,使颜色变深,能用勒夏特列原理解释,故D错误.
故选C.
点评:本题考查了勒夏特列原理的使用条件,难度不大,注意使用勒夏特列原理的前提必须是可逆反应.

练习册系列答案
 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
标准状况下有:①6.72LCH4②3.01×1023个HCl③10.8gH2O④0.7molNH3,下列对这四种气体的大小关系表示不正确的是( )
| A、体积:④>③>②>① |
| B、分子数:④>③>②>① |
| C、氢原子数:④>①=③>② |
| D、质量:②>④>③>① |
下列关于物质的量的说法,错误的是( )
| A、物质的量指的是物质所含构成粒子数的多少,它的单位是“摩尔” |
| B、1mol H2O含有6.02×1023个水分子 |
| C、1mol H2O的质量是18g |
| D、1mol H2O蒸汽的体积是22.4L |
设NA表示阿伏加德罗常数,下列说法中不正确的是( )
| A、标准状况下,22.4L氦气所含原子数为NA | ||
| B、2.3g金属钠变为钠离子时失去的电子数为0.1NA | ||
| C、常温常压下,44g CO2的质子数为15NA | ||
D、标准状况下,a L的氧气和氮气的混合物含有的分子数约为
|
下列几种物质中互为同位素的是( )
| A、水和重水 | B、氧气和臭氧 |
| C、石墨和金刚石 | D、氘和氚 |
 在450℃并有催化剂存在下,在体积为1L的密闭恒温容器中,二氧化硫和氧气发生如下反应:2SO2+O2?2SO3
在450℃并有催化剂存在下,在体积为1L的密闭恒温容器中,二氧化硫和氧气发生如下反应:2SO2+O2?2SO3 实验室制配0.5mol/L的NaOH溶液500mL.
实验室制配0.5mol/L的NaOH溶液500mL.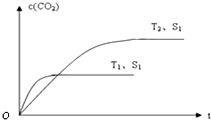 氮氧化物是空气的主要污染物,消除氮氧化物污染有多种方法.用催化技术可将超音速飞机尾气中的NO和CO转变成CO2和N2,其反应为:2NO+2CO?2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下测得不同时间的NO和CO浓度如下表:
氮氧化物是空气的主要污染物,消除氮氧化物污染有多种方法.用催化技术可将超音速飞机尾气中的NO和CO转变成CO2和N2,其反应为:2NO+2CO?2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下测得不同时间的NO和CO浓度如下表: