题目内容
6.在理论上可用于设计原电池的化学反应是( )| A. | 2Al(s)+2NaOH(aq)+2H2O(1)═2NaAlO2(aq)+3H2(g);△H<O | |
| B. | Ba(OH)2•8H2O(s)+2NH4Cl(s)═BaCl2(aq)+2NH3•H2O(aq)+8H2O(1);△H>0 | |
| C. | C3H8(g)+5O2(g)→4H2O (l)+3CO2(g);△H<0 | |
| D. | FeCl3(aq)十3H2O(1)?Fe(OH)3(s)+3HCl(aq);△H>0 |
分析 根据原电池的工作原理可以得出:自发的氧化还原反应可以设计成原电池,据此来回答.
解答 解:A、是放热反应,是氧化还原反应,能设计成原电池,故A正确;
B、属于复分解反应,是吸热反应,不是氧化还原反应,不能设计成原电池,故B错误;
C、是放热反应,是氧化还原反应,能设计成原电池,故C正确;
D、属于复分解反应,是吸热反应,不是氧化还原反应,不能设计成原电池,故D错误;
故选AC.
点评 本题是考查原电池的设计,难度不大,明确原电池的构成条件及反应必须是放热反应是解本题的关键.

练习册系列答案
相关题目
14.如图所示的实验中,能达到实验目的是( )
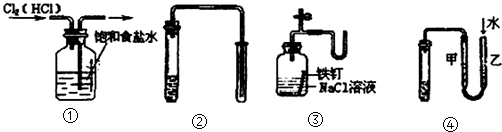
①除去Cl2中的HCl杂质②用铜和稀硝酸制取少量NO③证明铁生锈时空气参与反应④检验装置气密性.

①除去Cl2中的HCl杂质②用铜和稀硝酸制取少量NO③证明铁生锈时空气参与反应④检验装置气密性.
| A. | ①②③④ | B. | ③④ | C. | ②③④ | D. | ①④ |
1.已知X、Y是主族元素,I为电离能,单位是KJ/mol.根据下表所列数据判断错误的是:( )
| 元素 | I1 | I2 | I3 | I4 |
| X | 500 | 4600 | 6900 | 9500 |
| Y | 580 | 1800 | 2700 | 11600 |
| A. | 元素X的常见化合价是+1价 | |
| B. | 元素X的最高价氧化物对应水化物一定是强碱 | |
| C. | 元素Y是ⅢA族的元素 | |
| D. | 若元素Y处于第3周期,它可与冷水剧烈反应 |
11.NA代表阿伏加德罗常数的数值.下列有关NA的叙述中,正确的是( )
| A. | 1 mol 任何物质所含的分子数均为NA个 | |
| B. | 14 g氮气所含的N原子数为NA个 | |
| C. | 标准状况下,22.4 L水所含的H2O分子数为NA个 | |
| D. | 在钠与氯气的反应中,1 mol钠失去电子的数目为2 NA个 |
18.Al,Fe,Cu都是重要的金属元素.下列说法正确的是( )
| A. | 三者对应的氧化物均为碱性氧化物 | |
| B. | 三者的单质放置在空气中只生成氧化物 | |
| C. | 制备FeCl3不能采用将溶液直接蒸干的方法 | |
| D. | 电解AlCl3溶液是阴极上析出Al |
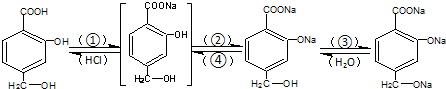
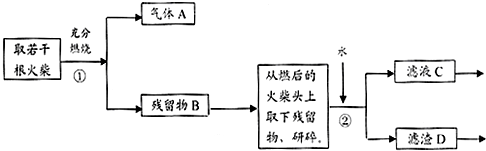
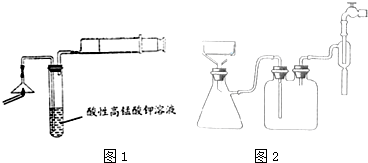
 NH3•H2O+H+.
NH3•H2O+H+. 2NH3(g)△H=-2a kJ mol-1.
2NH3(g)△H=-2a kJ mol-1.