题目内容
2.请设计实验方案区分已烷、溴乙烷、乙醇三种液态有机物.分析 乙醇易溶于水,溴乙烷不溶于水,且密度比水大,溴乙烷不溶于水,且密度比水大,可用水鉴别.
解答 解:乙醇易溶于水,溴乙烷不溶于水,且密度比水大,溴乙烷不溶于水,且密度比水大,则可取样,分别加入水中,漂浮在水面上方的是已烷,沉在水面下面的是溴乙烷,与水互溶的是乙醇,
答:取样,分别加入水中,漂浮在水面上方的是已烷,沉在水面下面的是溴乙烷,与水互溶的是乙醇.
点评 本题考查有机物的鉴别,侧重于有机物知识的综合考查以及实验方案的评价,注意把握有机物性质的异同,题目难度不大.

练习册系列答案
相关题目
17. 甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇:
甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇:
CO(g)+2H2(g)?CH3OH (g)
(1)在容积固定为2L的密闭容器内充入1mol CO和2mol H2,加入 催化剂后在250℃开始反应,CO的平衡转化率与温度、压强的关系如图所示.
容器中M、N两点气体的物质的量之比为5:4.
M、N、Q三点的平衡常数KM、KN、KQ的大小关系为KM=KN>KQ.
(2)通过压力计监测上述容器内压强的变化如下:
则从反应开始到20min时,以CO表示的平均反应速率为0.0125mol/(L.min),该温度下平衡常数K=4.
(3)下列描述中能说明上述反应已达平衡状态的是BC.
A.2v(H2)正=v(CH3OH)逆
B.容器内气体的平均摩尔质量保持不变
C.容器中气体的压强保持不变
D.单位时间内生成n mol CO的同时生成2n mol H2
(4)25℃时以甲醇燃料电池(电解质溶液为稀硫酸)为电源电解300mL NaCl溶液,正极反应式为O2+4 H++4 e-=2 H2O.在电解一段时间后,NaCl溶液的pH变为13(假设NaCl溶液的体积不变),则理论上消耗甲醇的物质的量为0.005mol.
 甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇:
甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇:CO(g)+2H2(g)?CH3OH (g)
(1)在容积固定为2L的密闭容器内充入1mol CO和2mol H2,加入 催化剂后在250℃开始反应,CO的平衡转化率与温度、压强的关系如图所示.
容器中M、N两点气体的物质的量之比为5:4.
M、N、Q三点的平衡常数KM、KN、KQ的大小关系为KM=KN>KQ.
(2)通过压力计监测上述容器内压强的变化如下:
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
| 压强/Mpa | 12.6 | 10.8 | 9.5 | 8.7 | 8.4 | 8.4 |
(3)下列描述中能说明上述反应已达平衡状态的是BC.
A.2v(H2)正=v(CH3OH)逆
B.容器内气体的平均摩尔质量保持不变
C.容器中气体的压强保持不变
D.单位时间内生成n mol CO的同时生成2n mol H2
(4)25℃时以甲醇燃料电池(电解质溶液为稀硫酸)为电源电解300mL NaCl溶液,正极反应式为O2+4 H++4 e-=2 H2O.在电解一段时间后,NaCl溶液的pH变为13(假设NaCl溶液的体积不变),则理论上消耗甲醇的物质的量为0.005mol.
14.由氢气和氧气反应生成1mol水蒸气放热241.8kJ,则反应2H2(g)+O2(g)$\frac{\underline{\;点燃\;}}{\;}$2H2O(g)的△H为( )
| A. | -483.6kJ•mol-1 | B. | -241.8kJ•mol-1 | C. | -120.6kJ•mol-1 | D. | +241.8kJ•mol-1 |
11.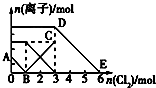 向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示.有关说法不正确的是( )
向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示.有关说法不正确的是( )
 向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示.有关说法不正确的是( )
向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示.有关说法不正确的是( )| A. | 线段BC代表Fe3+物质的量的变化情况 | |
| B. | 原混合溶液中n(FeBr2)=3mol | |
| C. | 当通入2molCl2时,溶液中已发生的离子反应为:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- | |
| D. | 原溶液中n(Fe2+):n(I-):n(Br-)=2:1:3 |
12.下列有关仪器的使用方法或实验操作不正确的是( )
| A. | 测定溶液pH时,pH试纸先用蒸馏水润湿 | |
| B. | 蒸馏实验中,蒸馏前必须在蒸馏烧瓶中加入碎瓷片 | |
| C. | 用盐酸滴定滴定氨水实验中,用甲基橙作指示剂以减小实验误差 | |
| D. |  用如图所示的方法排除碱式滴定管胶管中的气泡 用如图所示的方法排除碱式滴定管胶管中的气泡 |
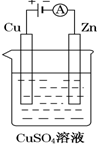 (1)合成氨反应的热化学方程式:N2(g)+3H2(g)═2NH3(g)△H=-92.2kJ•mol-1
(1)合成氨反应的热化学方程式:N2(g)+3H2(g)═2NH3(g)△H=-92.2kJ•mol-1 →合成→水热处理→过滤→水洗→表面处理→过滤水洗→干燥
→合成→水热处理→过滤→水洗→表面处理→过滤水洗→干燥