��Ŀ����
17�� �״���һ�����͵���������ȼ�ϣ���ҵ�Ͽ�ͨ��CO��H2�������Ʊ��״���
�״���һ�����͵���������ȼ�ϣ���ҵ�Ͽ�ͨ��CO��H2�������Ʊ��״���CO��g��+2H2��g��?CH3OH ��g��
��1�����ݻ��̶�Ϊ2L���ܱ������ڳ���1mol CO��2mol H2������ ��������250�濪ʼ��Ӧ��CO��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
������M��N������������ʵ���֮��Ϊ5��4��
M��N��Q�����ƽ�ⳣ��KM��KN��KQ�Ĵ�С��ϵΪKM=KN��KQ��
��2��ͨ��ѹ���Ƽ������������ѹǿ�ı仯���£�
| ��Ӧʱ��/min | 0 | 5 | 10 | 15 | 20 | 25 |
| ѹǿ/Mpa | 12.6 | 10.8 | 9.5 | 8.7 | 8.4 | 8.4 |
��3��������������˵��������Ӧ�Ѵ�ƽ��״̬����BC��
A��2v��H2����=v��CH3OH����
B�������������ƽ��Ħ���������ֲ���
C�������������ѹǿ���ֲ���
D����λʱ��������n mol CO��ͬʱ����2n mol H2
��4��25��ʱ�Լ״�ȼ�ϵ�أ��������ҺΪϡ���ᣩΪ��Դ���300mL NaCl��Һ��������ӦʽΪO2+4 H++4 e-=2 H2O���ڵ��һ��ʱ���NaCl��Һ��pH��Ϊ13������NaCl��Һ��������䣩�������������ļ״������ʵ���Ϊ0.005mol��
���� ��1��M��COת����Ϊ50%����ת����COΪ0.5mol���ɷ���ʽ��֪�������ʵ�����С0.5mol��2=1mol��������������ʵ���Ϊ��1+2-1��mol=2mol��N��COת����Ϊ70%����ת����COΪ0.7mol���ɷ���ʽ��֪�������ʵ�����С0.7mol��2=1.4mol��������������ʵ���Ϊ��1+2-1.4��mol=1.6mol��
��ͼ��֪�����¶����ߣ�CO��ת���ʼ�С��˵��ƽ�����淴Ӧ�����ƶ���ƽ�ⳣ����С��ƽ�ⳣ��֪ʶ�¶�Ӱ�죬�¶���ͬƽ�ⳣ����ͬ��
��2���ɱ������ݿ�֪��20minʱ����ƽ��״̬����ת����COΪx����
CO��g��+2H2��g��?CH3OH ��g��
��ʼ����mol����1 2 0
�仯����mol����x 2x x
ƽ������mol����1-x 2-2x x
ѹǿ֮�ȵ������ʵ���֮�ȣ���ƽ��ʱ������������ʵ���Ϊ��1mol+2mol����$\frac{8.4MPa}{12.6MPa}$=��1-x+2-2x��+x��mol�����x=0.5���ٸ���v=$\frac{��c}{��t}$����v��CO������ƽ�ⳣ��K=$\frac{c��C{H}_{3}OH��}{c��CO����{c}^{2}��{H}_{2}��}$��
��3��A����ͬ���ʱ�ʾ��������֮�ȵ��ڻ�ѧ������֮�ȣ���Ӧ����ƽ�⣻
B���������������ʵ�����С�ķ�����Ӧǰ�������ܵ������Dz���ģ�ֻҪ�������ƶ�����������Ħ�������ͻ�����
C���������������ʵ�����С�ķ����淴Ӧ���У�ѹǿ��С��ѹǿ���ٱ仯˵������ƽ�⣻
D����λʱ��������n mol CO��ͬʱ����2n mol H2������ʾ�淴Ӧ���ʣ���Ӧʼ�մ��ڸñ�����ϵ��
��4�������Ϸ�����ԭ��Ӧ��������������õ��ӣ���������������ˮ�����NaCl��Һ������Ӧ��2NaCl+2H2O$\frac{\underline{\;���\;}}{\;}$2NaOH+H2��+Cl2�����ڵ��һ��ʱ���NaCl��Һ��pH��Ϊ13����NaOHŨ��Ϊ0.1mol/L��������NaOHΪ0.3L��0.1mol/L=0.03mol��ȼ�ϵ���м״��������ɶ�����̼�����ݵ���ת���غ�������������ļ״������ʵ�����
��� �⣺��1��M��COת����Ϊ50%����ת����COΪ0.5mol���ɷ���ʽ��֪�������ʵ�����С0.5mol��2=1mol��������������ʵ���Ϊ��1+2-1��mol=2mol��N��COת����Ϊ70%����ת����COΪ0.7mol���ɷ���ʽ��֪�������ʵ�����С0.7mol��2=1.4mol��������������ʵ���Ϊ��1+2-1.4��mol=1.6mol��������M��N������������ʵ���֮��Ϊ2mol��1.6mol=5��4��
M��N�����¶���ͬ����KM=KN��KQ��ͼ��֪�����¶����ߣ�CO��ת���ʼ�С��˵��ƽ�����淴Ӧ�����ƶ���ƽ�ⳣ����С��Q����¶ȱ�M��N�ߣ���ƽ�ⳣ��KM=KN��KQ��
�ʴ�Ϊ��5��4��KM=KN��KQ��
��2���ɱ������ݿ�֪��20minʱ����ƽ��״̬����ת����COΪx����
CO��g��+2H2��g��?CH3OH ��g��
��ʼ����mol����1 2 0
�仯����mol����x 2x x
ƽ������mol����1-x 2-2x x
ѹǿ֮�ȵ������ʵ���֮�ȣ���ƽ��ʱ������������ʵ���Ϊ��1mol+2mol����$\frac{8.4MPa}{12.6MPa}$=��1-x+2-2x��+x��mol�����x=0.5��
��v��CO��=$\frac{\frac{0.5mol}{2L}}{20min}$=0.0125mol/��L��min����
ƽ�ⳣ��K=$\frac{c��C{H}_{3}OH��}{c��CO����{c}^{2}��{H}_{2}��}$=$\frac{\frac{0.5}{2}}{\frac{1-0.5}{2}����\frac{2-0.5��2}{2}��^{2}}$=4��
�ʴ�Ϊ��0.0125mol/��L��min����4��
��3��A����ͬ���ʱ�ʾ��������֮�ȵ��ڻ�ѧ������֮�ȣ���Ӧ����ƽ�⣬Ӧ��v��H2����=2v��CH3OH������ʾ��Ӧ����ƽ��״̬����A����
B���������������ʵ�����С�ķ�����Ӧǰ�������ܵ������Dz���ģ�ֻҪ�������ƶ�����������Ħ�������ͻ�����֮���С���ʻ������Ħ�������������˵������ƽ�⣬����ȷ��
C���������������ʵ�����С�ķ����淴Ӧ���У�ѹǿ��С��ѹǿ���ٱ仯˵������ƽ�⣬����ȷ��
D����λʱ��������n mol CO��ͬʱ����2n mol H2������ʾ�淴Ӧ���ʣ���Ӧʼ�մ��ڸñ�����ϵ���ʴ���
��ѡ��BC��
��4�������Ϸ�����ԭ��Ӧ��������������õ��ӣ���������������ˮ���缫��ӦʽΪ��O2+4 H++4 e-=2 H2O��
���NaCl��Һ������Ӧ��2NaCl+2H2O$\frac{\underline{\;���\;}}{\;}$2NaOH+H2��+Cl2�����ڵ��һ��ʱ���NaCl��Һ��pH��Ϊ13����NaOHŨ��Ϊ0.1mol/L��������NaOHΪ0.3L��0.1mol/L=0.03mol������������Ϊ0.015mol��ȼ�ϵ���м״��������ɶ�����̼�����ݵ���ת���غ㣬���������ļ״������ʵ���Ϊ$\frac{0.015mol��2}{6}$=0.005mol��
���ʴ�Ϊ��O2+4 H++4 e-=2 H2O��0.005mol��
���� ���⿼�黯ѧƽ����йؼ��㡢��ѧƽ��Ӱ�����ء���ѧƽ��״̬���жϡ��绯ѧ�ȣ����ؿ���ѧ�����������������Ѷ��еȣ�

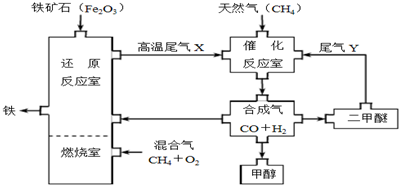
��1�����úϳ��������������У���ȼ����ͨ����������������������V��CH4����V��O2��Ϊ1��2��
��2��β��Y�ijɷ���ϳ���������йأ���ϳɶ�����ʱ�������ķ�Ӧ������2CO+4H2=CH3OCH3+H2O��3CO+3H2=CH3OCH3+CO2��
��3���ڴ���Ӧ�����������ķ�ӦΪ���淴Ӧ�����ѹ�����ѹ����ѹ���������ںϳ����ĺϳɣ�
��4����Cu2O/ZnOΪ�������ɺϳ����ϳɼ״�����һ���¶Ⱥ�ѹǿ���Է����У���Ӧ��CO��g��+2H2��g��?CH3OH��g���ڸ��¡���ѹ������һ�������Է����У�Ϊ̽���ϳɼ״��������¶Ⱥ�ѹǿ��ijͬѧ�������������ʵ�飺
| ʵ���� | n��H 2��/n��CO�� | T/�� | P/MPa |
| i | m1 | 250 | 1 |
| ii | 3 | T1 | 5 |
| iii | m2 | 350 | P1 |
| A�� | ͬ���ʵ���Ũ�ȵ�������Һ��pH��a��b��c | |
| B�� | ͬpHʱ��������Һϡ����ͬ������pH��a��b��c | |
| C�� | ͬpH��ͬ�����������Һ����ͬŨ������ �������a=b=c | |
| D�� | ͬpHʱ��ϡ�Ͳ�ͬ������pH����ͬ��������Һϡ�͵ı�����a��b��c |
| A�� | �ñ���ʳ��ˮ��ȥCl2��������HCl | |
| B�� | ����ˮ��ͨ��SO2���ɼ���SO2�Ļ�ԭ�Ժ�Ư���� | |
| C�� | ����Һ�������ᣬ������ɫ��ζ����ʹ����ʯ��ˮ���ǵ����壬������һ����CO2 | |
| D�� | �������ữ���Ȼ�����Һ����ij��Һ���Ƿ���SO42- |
 ��������0.4mol•L-1 NaOH ��Һ480mL��ijͬѧת����Һ��ʾ��ͼ��ͼ��
��������0.4mol•L-1 NaOH ��Һ480mL��ijͬѧת����Һ��ʾ��ͼ��ͼ��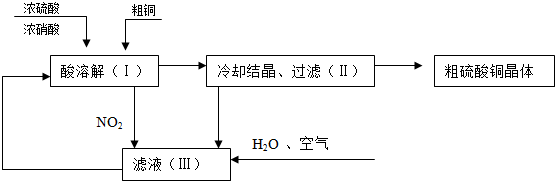

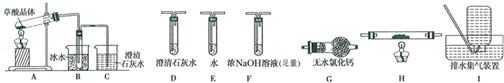
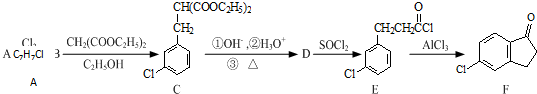
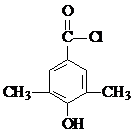 ��
��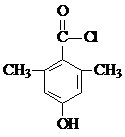 ����дһ�֣���
����дһ�֣���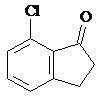 ��
��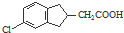 �ĺϳ�·������ͼ��ע����Ӧ���������ϳ�·������ͼʾ�����£�
�ĺϳ�·������ͼ��ע����Ӧ���������ϳ�·������ͼʾ�����£�