题目内容
【题目】氮是地球上含量丰富的一种元素,其单质及化合物在工农业生产、生活中有着重要作用。
(1)如图是1mol NO2(g)和 1mol CO(g)反应生成 1mol CO2(g)和 1mol NO(g)过程中能量变化示意图。

①该反应是_________(填“吸热”或 “放热”)反应。
②请写出反应的热化学方程式_________。
③若在该反应体系中加入催化剂对反应热_________(填“有”或“没有”)影 响。原因是_________。
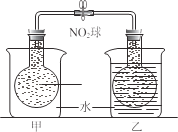
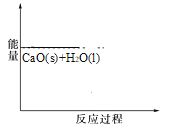
(2)已知,可逆反应2NO2 (g)N2O4 (g) ΔH=56.9 kJ/mol。在乙烧杯中投入一定量的CaO固体,此烧杯中NO2球的红棕色变深。根据现象,补全CaO与H2O反应过程的能量变化示意图_________。
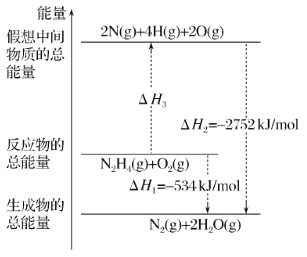
(3)肼(N2H4)是一种应用广泛的化工原料,可作为火箭发动机的燃料。已知断裂 1 mol 化学键所需的能量:N≡N 为 942 kJ、O=O 为 500 kJ、N-N 为154 kJ,则断裂 1 mol N-H 键所需的能量是_________。
【答案】放热 ![]() 没有 反应热只与反应的始态和终态有关,与反应的途径无关
没有 反应热只与反应的始态和终态有关,与反应的途径无关 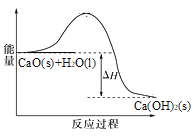 391kJ
391kJ
【解析】
(1)①根据反应过程图示,可知反应物的总能量高于生成物的总能量,故该反应是放热反应,故答案为:放热;
②从图中可知,该反应的反应热为![]() ,故该反应的热化学方程式为
,故该反应的热化学方程式为![]() ,故答案为:
,故答案为:![]() ;
;
③由于反应热与反应途径无关,只与反应的始态和终态有关,加入催化剂对反应热没有影 响,故答案为:没有 反应热只与反应的始态和终态有关,与反应的途径无关
(2)乙烧杯中NO2球的红棕色变深,说明2NO2(g)N2O4(g) ΔH=56.9 kJ/mol平衡向逆方向移动,而该反应是一个放热反应,故说明CaO与H2O的反应是一个放热反应,使乙烧杯中的温度升高,故反应过程的能量变化示意图为: ,故答案为:
,故答案为: ;
;
(3)根据图示,N2H4(g)+O2(g)=N2(g)+2H2O(g) H1=-534kJ/mol,由图可知,反应过程如下: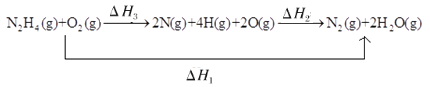 ,由盖斯定律可知:H1=H2+H3,H3=-534kJ/mol-(-2752kJ/mol)=2218kJ/mol,即4E(N—H)+E(N—N)+E(O=O)=2218kJ/mol,代入数据即可求出E(N—H)=391kJ/mol,故答案为:391kJ。
,由盖斯定律可知:H1=H2+H3,H3=-534kJ/mol-(-2752kJ/mol)=2218kJ/mol,即4E(N—H)+E(N—N)+E(O=O)=2218kJ/mol,代入数据即可求出E(N—H)=391kJ/mol,故答案为:391kJ。

 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案【题目】中学化学教材中,常借助于图像这一表现手段清晰地突出实验装置的要点、形象地阐述化学过程的原理。下列有关化学图像表现的内容不正确的是
选项 | A | B | C | D |
装置 |
|
|
|
|
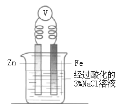
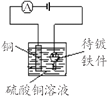
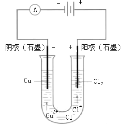
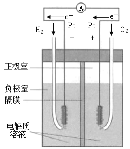
原理 | 牺牲阳极的阴极保护法 | 电镀 | 电解CuCl2溶液 | 氢氧燃料电池 |
A.AB.BC.CD.D
【题目】在2L密闭容器中进行反应![]() ,式中m、n、p、q为化学计量数。在
,式中m、n、p、q为化学计量数。在![]() min内,各物质物质的量的变化如下表所示:
min内,各物质物质的量的变化如下表所示:
物质 时间 | X | Y | Z | Q |
起始/mol | 0.7 | 1 | ||
2min末/mol | 0.8 | 2.7 | 0.8 | 2.7 |
3min末/mol | 0.8 |
已知2min内![]() ,
,![]() ,试确定以下物质的相关量:
,试确定以下物质的相关量:
(1)起始时![]() __________,
__________,![]() __________。
__________。
(2)方程式中m=__________,n=__________,p=__________,q=__________。
(3)用Z表示2min内的反应速率:____________________。