题目内容
7.Y、Z三种金属,X、Y组成原电池,X是负极;把Z放入X的硝酸盐溶液中,Z表面有X析 出.三者的金属活动性顺序是( )| A. | X>Y>Z | B. | Z>X>Y | C. | X>Z>Y | D. | Y>X>Z |
分析 活泼性强的金属可以把活泼性弱的金属从其盐中置换出来,原电池中,负极金属的活泼性强于正极金属的活泼性.
解答 解:X、Y组成原电池,X是负极,所以活泼性X>Y;把Z放入X的硝酸盐溶液中,Z表面有X析出,说明金属Z可以把金属X从其盐中置换出来,所以活泼性Z>X,所以X、Y、Z三种金属的活动性顺序为Z>X>Y.
故选B.
点评 本题考查判断金属活泼性的方法,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
15. 一定温度下,向容积为2L的恒容密闭容器中充入6mol CO2和8mol H2,发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1,测得n(H2)随时间变化如曲线Ⅰ所示.下列说法正确的是( )
一定温度下,向容积为2L的恒容密闭容器中充入6mol CO2和8mol H2,发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1,测得n(H2)随时间变化如曲线Ⅰ所示.下列说法正确的是( )
 一定温度下,向容积为2L的恒容密闭容器中充入6mol CO2和8mol H2,发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1,测得n(H2)随时间变化如曲线Ⅰ所示.下列说法正确的是( )
一定温度下,向容积为2L的恒容密闭容器中充入6mol CO2和8mol H2,发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1,测得n(H2)随时间变化如曲线Ⅰ所示.下列说法正确的是( )| A. | 该反应在0~8 min内CO2的平均反应速率是 0.375 mol•L-1•min-1 | |
| B. | 若起始时向上述容器中充入3 mol CO2和4 mol H2,则平衡时H2的体积分数大于20% | |
| C. | 若起始时向上述容器中充入4 mol CO2、2 mol H2、2 mol CH3OH和1mol H2O(g),则此时反应向正反应方向进行 | |
| D. | 改变条件得到曲线Ⅱ、Ⅲ,则曲线Ⅱ、Ⅲ改变的条件分别是升高温度、充入氦气 |
18.设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 标准状况下,11.2LSO3所含的原子数为1.5NA | |
| B. | 常温常压下,1.8g H2O中含有的电子数为0.8NA | |
| C. | 常温常压下,48g O2和O3的混合物中含有的氧原子数为3NA | |
| D. | 标准状况下,0.1mol Cl2与足量NaOH溶液反应时,转移的电子数为0.2NA |
15.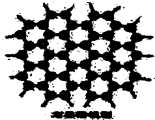 石墨晶体是层状结构,在每一层里,每一个碳原子都跟其它3个碳原子相结合.如图是石墨的晶体结构俯视图,图中每个黑点表示1个碳原子,而两黑点间的连线表示1个共价键,则石墨晶体中碳原子个数与共价键个数之比为( )
石墨晶体是层状结构,在每一层里,每一个碳原子都跟其它3个碳原子相结合.如图是石墨的晶体结构俯视图,图中每个黑点表示1个碳原子,而两黑点间的连线表示1个共价键,则石墨晶体中碳原子个数与共价键个数之比为( )
 石墨晶体是层状结构,在每一层里,每一个碳原子都跟其它3个碳原子相结合.如图是石墨的晶体结构俯视图,图中每个黑点表示1个碳原子,而两黑点间的连线表示1个共价键,则石墨晶体中碳原子个数与共价键个数之比为( )
石墨晶体是层状结构,在每一层里,每一个碳原子都跟其它3个碳原子相结合.如图是石墨的晶体结构俯视图,图中每个黑点表示1个碳原子,而两黑点间的连线表示1个共价键,则石墨晶体中碳原子个数与共价键个数之比为( )| A. | 1:3 | B. | 2:3 | C. | 2:1 | D. | 3:2 |
2.已知X、Y为同周期元素,且第一电离能X<Y,下列说法中正确的是( )
| A. | 电负性:X<Y | |
| B. | 周期表中,X可能在Y的右边 | |
| C. | 若X与Y形成化合物,则X显正价,Y显负价 | |
| D. | 气态氢化物的稳定性:HmY强于HnX |
12.区别CH3CH2CH2OH与 的方法是( )
的方法是( )
 的方法是( )
的方法是( )| A. | 加入金属钠 | |
| B. | 加银氨溶液 | |
| C. | 在铜存在下和氧气反应 | |
| D. | 在铜存在下和氧气反应后的产物中加入银氨溶液共热 |
19.如图所示,在较高温度时,钾、氧两元素形成的一种晶体结构与NaCl晶体结构相似,则该化合物的化学式为( )
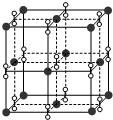

| A. | KO2 | B. | K2O2 | C. | K2O3 | D. | K2O |
16.下列物质的电子式书写正确的是( )
| A. | 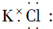 | B. |  | ||
| C. | 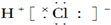 | D. | 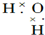 |