题目内容
【题目】温度为T时,在两个起始容积都为1L的恒温密闭容器发生反应:H2(g)+I2(g) ![]() 2HI(g) ΔH<0。实验测得:v正=v(H2)消耗=v(I2)消耗=k正c(H2)·c(I2),v逆=v(HI)消耗=k逆c2 (HI),k正、k逆为速率常数,受温度影响。下列说法正确的是
2HI(g) ΔH<0。实验测得:v正=v(H2)消耗=v(I2)消耗=k正c(H2)·c(I2),v逆=v(HI)消耗=k逆c2 (HI),k正、k逆为速率常数,受温度影响。下列说法正确的是
容器 | 物质的起始浓度(mol·L-1) | 物质的平衡浓度 | ||
c(H2) | c(I2) | c(HI) | ||
Ⅰ(恒容) | 0.1 | 0.1 | 0 | c(I2)=0.07 mol·L-1 |
Ⅱ(恒压) | 0 | 0 | 0.6 | |
A. 反应过程中,容器Ⅰ与容器Ⅱ中的总压强的比为1:3
B. 两容器达平衡时:c(HI,容器Ⅱ)>3c(HI,容器Ⅰ)
C. 温度一定,容器Ⅱ中反应达到平衡时(平衡常数为K),有K=![]() 成立
成立
D. 达平衡时,向容器Ⅰ中同时再通入0.1 mol I2和0.1 mol HI,则此时ν正>ν逆
【答案】AC
【解析】该反应为气体体积不变的反应,根据表中数据可知,以上两容器中反应为等温等压下的等效平衡,A.假设能按比例完全转化为HI,则容器Ⅰ与容器Ⅱ的物质的量之比为1:3,体积相同,则反应过程中,容器Ⅰ与容器Ⅱ中的总压强的比为1:3,选项A正确;B、两容器达平衡时:c(HI,容器Ⅱ)=3c(HI,容器Ⅰ),B错误;C、温度一定,容器Ⅱ中反应达到平衡时v正=v逆,由v正=v(H2)消耗=v(I2)消耗=k正c(H2)·c(I2)得c(H2)·c(I2)= ![]() ,由v逆=v(HI)消耗=k逆c2 (HI)得c2 (HI)=
,由v逆=v(HI)消耗=k逆c2 (HI)得c2 (HI)= ![]() ,则有K=
,则有K=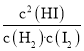 =
=![]() =
=![]() ,选项C正确;D、容器Ⅰ达平衡时,H2、I2、HI的浓度分别为0.07 mol·L-1、0.07 mol·L-1、0.03 mol·L-1,K=
,选项C正确;D、容器Ⅰ达平衡时,H2、I2、HI的浓度分别为0.07 mol·L-1、0.07 mol·L-1、0.03 mol·L-1,K=![]() ,向容器Ⅰ中同时再通入0.1 mol I2和0.1 mol HI,则此时Q=
,向容器Ⅰ中同时再通入0.1 mol I2和0.1 mol HI,则此时Q=![]() >K,ν逆>ν正,选项D错误。答案选AC。
>K,ν逆>ν正,选项D错误。答案选AC。

【题目】1915年诺贝尔物理学奖授予Henry Bragg 和 Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献。
(1)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如下表:
晶体 | NaCl | KCl | CaO |
晶格能/(kJ·mol1) | 786 | 715 | 3401 |
四种晶体NaCl、KCl、MgO、CaO熔点由高到低的顺序是______,Na核外有__________种不同的能级。
(2)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可用右图简单表示,其中配位键和氢键均采用虚线表示。

①SO42 中S的杂化类型是____________,与其互为等电子体的离子有___________(任写两种)
②已知 [Cu(NH3)4]2+ 具有对称的空间构型,[Cu(NH3)4]2+ 中的两个NH3被 Cl 取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为_______________。
③写出基态Cu2+ 的价层电子排布式:_________;金属铜采取_________堆积方式,已知Cu原子的半径为 r pm,NA 表示阿伏加德罗常数的值,金属铜的密度是_______________g/cm3(列出计算式)