题目内容
20.下列说法正确的是( )| A. | 将苯和溴水混合后加入铁粉制取湨苯 | |
| B. | 检验溴乙烷中的湨元素的方法是加入NaOH溶液共热,冷却后滴入AgNO3溶液,观察有无浅黄色沉淀生成 | |
| C. | 将硝酸银溶液加入到浓氨水中配成银氨溶液后,滴加几滴乙醛加热煮沸制银镜 | |
| D. | 蒸馏操作中,将温度计放置在蒸馏烧瓶支管口附近 |
分析 A.苯与溴水不反应;
B.水解后检验溴离子,应在酸性条件下;
C.将氨水滴加到硝酸银溶液中,至最初生成的沉淀恰好溶解制备银氨溶液;
D.蒸馏时,温度计测定馏分的温度.
解答 解:A.苯与溴水不反应,应利用苯、液溴混合后加入铁粉制取湨苯,故A错误;
B.水解后检验溴离子,应在酸性条件下,则水解后加硝酸至酸性,再冷却后滴入AgNO3溶液,观察有无浅黄色沉淀生成,故B错误;
C.将氨水滴加到硝酸银溶液中,至最初生成的沉淀恰好溶解制备银氨溶液,试剂顺序不合理,故C错误;
D.蒸馏时,温度计测定馏分的温度,则温度计放置在蒸馏烧瓶支管口附近,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握有机物的制备实验、性质实验、混合物分离提纯实验等为解答的关键,侧重分析与实验能力的考查,注意实验评价性分析及实验技能,题目难度不大.

练习册系列答案
相关题目
10.在化学研究中,人们经常需要根据不同原子、分子或离子的某些特征反应对物质进行检验,以确定物质的组成.下列有关物质检验的说法不正确的是( )
| A. | 可以用BaCl2溶液和稀硝酸检验Na2SO3是否变质 | |
| B. | 某溶液中滴入KSCN溶液后变红,说明溶液中存在Fe3+ | |
| C. | MnO2、CuO、Fe三种物质的粉末都是黑色的,用稀盐酸能将它们区别开 | |
| D. | 用湿润的KI淀粉试纸可以检验氯化氢气体中是否含有氯气 |
11.下列化合物中,含有共价键的离子化合物是( )
| A. | CaCl2 | B. | O2 | C. | H2O | D. | NH4NO3 |
8.下列对部分化学知识的归纳完全正确的一组是( )
| A. | 化学与生活 ①生活中常用加热煮沸的方法软化硬水 ②用燃烧的方法区分羊毛和涤纶 ③干冰用于人工降雨 | |
| B. | 化学与环境 ①焚烧植物秸秆不会造成空气污染 ②PM2.5是造成雾霾天气的元凶之一 ③含磷洗涤剂的使用会导致水污染 | |
| C. | 化学与安全 ①炒菜油锅着火可以用锅盖盖灭 ②在室内放一盆水,可防止煤气中毒 ③夜间发现液化气泄漏开灯寻找泄漏源 | |
| D. | 化学与健康 ①人体缺铁会引起贫血 ②用甲醛的水溶液浸泡海产品保鲜 ③食用蔬菜和水果来补充维生素 |
5.下列化学用语书写正确的是( )
| A. | 乙烯的结构简式:CH2CH2 | B. | 次氯酸的结构式:H-O-Cl | ||
| C. | NH4Cl的电子式: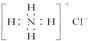 | D. | 硝基苯的结构简式: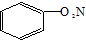 |
12.下列反应属于取代反应是( )
| A. | 2KI+Cl2═2KCl+I2 | B. | C2H5Cl+H2O C2H5OH+HCl C2H5OH+HCl | ||
| C. | nCH2═CH2$\stackrel{催化剂}{→}$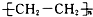 | D. | 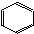 +3H2$→_{△}^{催化剂}$ +3H2$→_{△}^{催化剂}$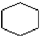 |
9.常见物质的电离平衡常数如下表,下列离子反应方程式错误的是( )
| 物质 | H2CO3 | HClO | HAlO2 |
| 电离常数 (25℃) | Ka1=4.4×10-7 | Ka=3×10-8 | Ka=6.3×10-13 |
| Ka2=4.7×10-11 |
| A. | NaClO溶液中通入过量CO2:ClO-+CO2+H2O═HClO+HCO3- | |
| B. | NaClO溶液中通入少量CO2:2ClO-+CO2+H2O═2HClO+CO32- | |
| C. | NaAlO2溶液中加入过量CO2:AlO2-+CO2+2H2O═HCO3-+Al(OH)3↓ | |
| D. | NaAlO2溶液中通入少量CO2:2AlO2-+CO2+3H2O═CO32-+2Al(OH)3↓ |
10.a、b、c、d为短周期元素,a的M电子层有1个电子,b的最外层电子数为内层电子数的2倍,c的最高化合价为最低化合价绝对值的3倍,c与d同周期,d的原子半径小于c.下列叙述不正确的是( )
| A. | a与其他元素生成的化合物都是离子化合物 | |
| B. | b与氢形成的所有化合物中化学键均为极性共价键 | |
| C. | c存在两种或两种以上的氧化物 | |
| D. | 在四种元素中,d元素的非金属性最强 |

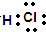 ,其中所含化学键的类型是共价键.
,其中所含化学键的类型是共价键.