题目内容
13.不同元素的原子,一定具有不同的( )| A. | 质量数 | B. | 质子数 | C. | 中子数 | D. | 电子数 |
分析 根据元素的种类由质子数来决定,则不同元素的原子或离子质子数一定不同,中子数可能相同,也可能不同,再根据质量数=质子数+中子数,可知质量数可能相同,也可能不同.
解答 解:元素的种类由质子数来决定,则不同元素的原子或离子质子数一定不同,中子数可能相同,也可能不同,如136C和147N,126C和147N;
再根据质量数=质子数+中子数,可知质量数可能相同,也可能不同,如136C和147N,146C和147N;
所以不同元素的原子,一定具有不同的质子数,
故选B.
点评 本题考查元素的种类由质子数决定以及各微粒之间的关系,难度不大,注意举例说明.

练习册系列答案
相关题目
10.下列有关化学用语正确的是( )
| A. | 26Fe的价层电子排布式为3d64s2 | |
| B. | 35Br的电子排布式可简写为[Ar]4s24p5 | |
| C. | NH4Cl的电子式为 | |
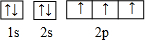
| D. | 某基态原子核外电子排布图为: |
1.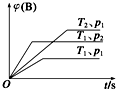 已知某可逆反应mA(g)+nB(g)?qC(g)△H在密闭容器中进行.如图表示在不同时刻t、温度T和压强p下B物质在混合气体中的体积分数φ(B)的变化情况.下列推断中正确的是( )
已知某可逆反应mA(g)+nB(g)?qC(g)△H在密闭容器中进行.如图表示在不同时刻t、温度T和压强p下B物质在混合气体中的体积分数φ(B)的变化情况.下列推断中正确的是( )
 已知某可逆反应mA(g)+nB(g)?qC(g)△H在密闭容器中进行.如图表示在不同时刻t、温度T和压强p下B物质在混合气体中的体积分数φ(B)的变化情况.下列推断中正确的是( )
已知某可逆反应mA(g)+nB(g)?qC(g)△H在密闭容器中进行.如图表示在不同时刻t、温度T和压强p下B物质在混合气体中的体积分数φ(B)的变化情况.下列推断中正确的是( )| A. | p1>p2,T1<T2,m+n>q,△H<0 | B. | p1<p2,T1>T2,m+n>q,△H<0 | ||
| C. | p1>p2,T1<T2,m+n<q,△H<0 | D. | p1<p2,T1>T2,m+n<q,△H>0 |
8.下列化学用语正确的是( )
| A. | 氯化钠的电子式 | B. | 氢气的结构式H=H | ||
| C. | 磷原子的结构示意图 | D. | 乙酸的分子式C2H4O2 |
18.下列说法正确的是( )
| A. | 石油裂解、煤的气化、海水制镁等过程中都包含化学变化 | |
| B. | 通过化学变化可以实现235U与238U的相互转化 | |
| C. | 煤经气化、液化和干馏三个物理变化过程,可变为清洁能源 | |
| D. | 明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理相同 |
5.下列表示物质结构的化学用语正确的是( )
| A. | 乙烯的结构简式:CH2CH2 | B. | NaCl的电子式: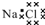 | ||
| C. | Cl-的结构示意图: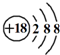 | D. | CH4的比例模型: |
3.下列各组物质中,都是弱电解质的是( )
| A. | HBr、HCl、AgCl | B. | CaCO3、CH3COONa、NaHSO4 | ||
| C. | HClO、HF、NH3 | D. | H2CO3、CH3COOH、H2S |
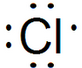 .
.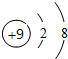 .
.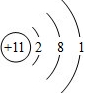 D2-的电子式为
D2-的电子式为 .
. ;Z元素原子的电子式为
;Z元素原子的电子式为 .
.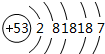 .
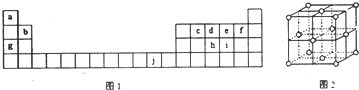
.
 .
.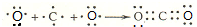 ,1molce2含有σ键的数目为6.02×1023.
,1molce2含有σ键的数目为6.02×1023.