题目内容
5.下列表示物质结构的化学用语正确的是( )| A. | 乙烯的结构简式:CH2CH2 | B. | NaCl的电子式: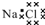 | ||
| C. | Cl-的结构示意图: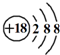 | D. | CH4的比例模型: |
分析 A.结构简式中需要标出官能团结构,乙烯分子中含有碳碳双键;
B.氯化钠为离子化合物,阴阳离子需要标出所带电荷,氯离子还要标出最外层电子;
C.氯离子的核电荷数为17,不是18;
D.甲烷为正四面体结构,碳原子半径大于氢原子.
解答 解:A.乙烯分子中存在碳碳双键,乙烯正确的结构简式:CH2=CH2,故A错误;
B.氯化钠为离子化合物,离子化合物的电子式中需要标出电荷,氯化钠的电子式为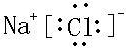 ,故B错误;
,故B错误;
C.氯离子核电荷数为17,核外电子数为18,氯离子正确的结构示意图为: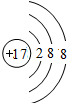 ,故C错误;
,故C错误;
D.甲烷分子中含有4个碳氢键,碳原子半径大于氢原子,甲烷的比例模型为: ,故D正确;
,故D正确;
故选D.
点评 本题考查了常见化学用语的表示方法,他题目难度中等,涉及电子式、离子结构示意图、比例模型、结构简式等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.

练习册系列答案
相关题目
2.下列玻璃仪器中,能用于加热的有( )
| A. | 烧杯 | B. | 容量瓶 | C. | 量筒 | D. | 试剂瓶 |
16.如图是验证某气体化学性质的实验装置,如打开B,从A处通干燥的氯气,C中干燥的红色布条无变化,如关闭B,C中干燥的红色布条褪色,则D中 所装溶液是( )
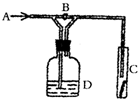

| A. | 浓H2SO4 | B. | 饱和NaCl溶液 | C. | NaOH溶液 | D. | NaBr溶液 |
13.不同元素的原子,一定具有不同的( )
| A. | 质量数 | B. | 质子数 | C. | 中子数 | D. | 电子数 |
20.下列说法正确的是( )
| A. | 将标准状况下的2.24L CO2通入150mL 1mol•L-1 NaOH溶液中,所得溶液中c(CO32-)>c(HCO3-) | |
| B. | 常温下0.1 mol•L-1的下列溶液①NH4Al(SO4)2 ②NH4Cl ③NH3•H2O④CH3COONH4中,c(NH4+)由大到小的顺序是:②>①>④>③ | |
| C. | 0.1 mol•L-1 pH为9的NaHB溶液中:c(HB-)>c(B2-)>c(H2B) | |
| D. | 室温下,将0.4mol/L HA溶液和0.2mol/LNaOH溶液等体积混合(忽略混合时溶液体积的变化)测得混合液pH=5,则c(A-)+c (OH-)>c(H+)+c(HA) |
17.下列反应过程符合如图所示关系的是( )
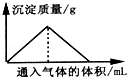

| A. | 向漂白粉溶液中通入CO2气体至过量 | |
| B. | 向Na2SiO3溶液中通入HCl气体至过量 | |
| C. | 向Ba(OH)2和KOH混合溶液中通入CO2气体至过量 | |
| D. | 向NaAlO2溶液中通入HCl气体至过量 |
14.5.6g铁粉投入到足量的100mL2mol/L的稀硫酸中,2min时铁粉刚好溶解,下列表示这个反应的速率正确的是( )
| A. | v(Fe)=0.5mol/(L•min) | B. | v(H2SO4)=0.5mol/(L•min) | ||
| C. | v(H2)=0.5mol/(L•min) | D. | v(FeSO4)=0.5mol/(L•min) |
15.两种金属粉末的混合物9g与足量的稀硫酸反应收集到标准状况下的氢气6.72L,则这种混合物的可能组成是( )
| A. | Mg和Al | B. | Fe和Zn | C. | Fe和Cu | D. | Fe和Al |