题目内容
2.某化学研究性学习小组对含有杂质的铜粉进行分析(杂质不与稀硝酸反应).取2.4g样品与20mL的稀硝酸充分反应,生成气体为448mL(已换算为标准状况下).(1)该样品中所含杂质的质量为0.48g.
(2)反应后的溶液中氢离子的浓度为4mol/L(上述反应前后体积不变),现用2mol/L的NaOH溶液滴加至铜离子恰好全部转化为Cu(OH)2沉淀,需消耗NaOH溶液的体积为100mL.
分析 铜与稀硝酸反应的实质是3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,在溶液中每3molCu与8molH+完全反应生成2molNO气体,而生成气体的体积为448mL,物质的量为:$\frac{448×1{0}^{-3}L}{22.4L/mol}$=0.02mol,所以溶液中铜的物质的量为:0.03mol,恰好完全沉淀得到单一的硝酸钠由此分析解答.
解答 解:铜与稀硝酸反应的实质是3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,在溶液中每3molCu与8molH+完全反应生成2molNO气体,而生成气体的体积为448mL,物质的量为:$\frac{448×1{0}^{-3}L}{22.4L/mol}$=0.02mol,所以溶液中铜的物质的量为:0.03mol,
(1)该样品中所含杂质的质量为2.4g-0.03mol×64g/mol=0.48g,故答案为:0.48;
(2)根据电荷守恒可知:2c(Cu2+)+c(H+)=c(NO3-),c(NO3-)=2×$\frac{0.03}{0.02}$+4=10mol/L,所以n(NaOH)=n(NaNO3)=n(NO3-)=10×0.02=0.2mol,所以V(NaOH)=$\frac{0.2mol}{2mol/L}$=0.1L=100mL,故答案为:100.
点评 本题主要考查硝酸的化学性质、化学方程式的过量计算,主要考查了学生要掌握有关物质的量之间的转化的同时,还要会熟练掌握电荷守恒的应用.

练习册系列答案
相关题目
13.2015年12月12日,第21届联合国巴黎气候变化大会通过全球气候变化新协议.协议要求各国减少工业排放量的气体是( )
| A. | 二氧化硫 | B. | 氮的氧化物 | C. | 二氧化碳 | D. | 臭氧 |
17.下列物质的水溶液因水解呈碱性的是( )
| A. | NaOH | B. | CH3COONa | C. | NH4Cl | D. | NaHSO4 |
7.苯甲酸广泛应用于制药和化工行业,某同学尝试用甲苯的氧化反应制备苯甲酸,反应原理:
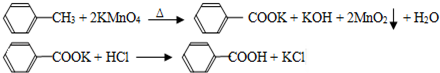
实验方法:一定量的甲苯和KMnO4溶液在100℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯.
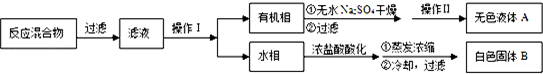
已知:苯甲酸分子量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3g和6.9g;纯净固体有机物都有固定熔点.
(1)操作Ⅰ为分液,操作Ⅱ为蒸馏.
(2)无色液体A是甲苯,定性检验A的试剂是酸性KMnO4溶液,现象是紫色溶液褪色.
(3)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确.请在答题卡上完成表中内容.
(4)纯度测定:称取1.220g产品,配成100ml甲醇溶液,移取25.00ml溶液,滴定,消耗KOH的物质的量为2.40×10-3mol,产品中苯甲酸质量分数为96%(保留二位有效数字).

实验方法:一定量的甲苯和KMnO4溶液在100℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯.

已知:苯甲酸分子量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3g和6.9g;纯净固体有机物都有固定熔点.
(1)操作Ⅰ为分液,操作Ⅱ为蒸馏.
(2)无色液体A是甲苯,定性检验A的试剂是酸性KMnO4溶液,现象是紫色溶液褪色.
(3)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确.请在答题卡上完成表中内容.
| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 将白色固体B加入水中,加热溶 解,冷却、过滤 | 得到白色晶体和无色溶液 | ----------------- |
| ② | 取少量滤液于试管中,滴入适量的硝酸酸化的AgNO3溶液 | 生成白色沉淀 | 滤液含Cl- |
| ③ | 干燥白色晶体,加热使其融化,测其熔点 | 熔点为122.4℃ | 白色晶体是苯甲酸 |
14.下列说法错误的是( )
| A. | 液氨汽化时要吸收大量的热,常用作制冷剂 | |
| B. | 压减燃煤、严格控车、调整产业是治理雾霾的有效措施 | |
| C. | 手机外壳上贴的碳纤维外膜是一种新型的无机非金属材料 | |
| D. | 铝及其合金是电气、工业、家庭广泛使用的材料,是因为铝比铁更耐酸碱的腐蚀 |
 硫代硫酸钠晶体(Na2S203•5H20)俗名“大苏打”.己知它易溶于水,难溶于乙醇,加热和遇酸易分解.某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如图:
硫代硫酸钠晶体(Na2S203•5H20)俗名“大苏打”.己知它易溶于水,难溶于乙醇,加热和遇酸易分解.某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如图: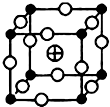 卤族元素是典型的非金属元素,卤素单质及其化合物在生产和生活中都有重要的用途.
卤族元素是典型的非金属元素,卤素单质及其化合物在生产和生活中都有重要的用途. 、
、 、
、 分别代表一种离子),晶胞边长为anm(1nm=10-9m),该晶体的化学式为KMgF3,该晶体的密度为$\frac{0.1993}{{a}^{3}}$g•cm-3.
分别代表一种离子),晶胞边长为anm(1nm=10-9m),该晶体的化学式为KMgF3,该晶体的密度为$\frac{0.1993}{{a}^{3}}$g•cm-3.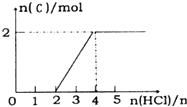 A、B、C、D、E 分别代表中学化学中的常见物质,请根据题目要求回答下列问题:
A、B、C、D、E 分别代表中学化学中的常见物质,请根据题目要求回答下列问题: .
. .
.