题目内容
17.如图甲、乙是电化学实验装置.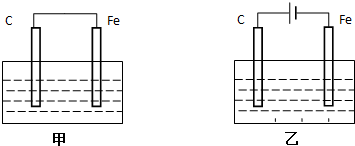
(1)若甲、乙两烧杯中均盛有饱和NaCl溶液.
①甲中碳棒上的电极反应式为2H2O+O2+4e-═4OH-;
②乙中碳棒上的电极反应式为2Cl--2e-=Cl2↑;乙中总反应的离子方程式为2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑+2OH-_;
③将湿润的淀粉-KI试纸放在乙烧杯上方,发现试纸先变蓝后褪色,这是因为过量的Cl2氧化了生成的I2.若反应中Cl2和I2的物质的量之比为5:1,且生成两种酸,该反应的化学方程式为:5Cl2+I2+6H2O═10HCl+2HIO3.
(2)若甲、乙两烧杯中均盛有CuSO4溶液.
①甲中铁棒上的电极反应式为Fe-2e-═Fe2+;
②如果起始时乙中盛有200 mL pH=5的CuSO4溶液(25℃),一段时间后溶液的pH变为1,若要使溶液恢复到电解前的状态,可向溶液中加入CuO(或CuCO3)(填写物质的化学式)0.8(或1.24)g(电解前后溶液的体积不变).
分析 (1)①甲为原电池装置,铁作负极,则石墨作正极,正极上氧气得电子;
②乙为电解装置,由电子流向可知石墨为阳极,阳极上氯离子放电,阴极上氢离子放电;
③Cl2氧化了生成的I2,Cl元素的化合价降低,由电子守恒及Cl2和I2的物质的量之比为5:1来判断反应后I元素的化合价,以此来书写化学反应;
(2)①甲为原电池装置,铁作负极,铁失电子;
②根据电解硫酸铜的化学反应及元素守恒来判断加入的物质使溶液恢复到电解前的状态,再由溶液的pH的变化计算加入物质的质量.
解答 解:(1)①甲为原电池装置,石墨棒上氧气得电子发生还原反应,反应为2H2O+O2+4e-═4OH-,
故答案为:2H2O+O2+4e-═4OH-;
②乙为电解装置,由电源可知C棒为阳极,阳极上氯离子放电,即2Cl--2e-=Cl2↑,阴极上氢离子放电,则电解反应为2Cl-+2H2O $\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑+2OH-,故答案为:2Cl--2e-=Cl2↑;2Cl-+2H2O $\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑+2OH-;
③Cl2氧化了生成的I2,Cl元素的化合价降低,生成盐酸,反应中Cl2和I2的物质的量之比为5:1,设I元素的化合价为x,则5×2×1=1×2×x,解得x=+5,则生成碘酸,所以发生的化学反应为5Cl2+I2+6H2O═10HCl+2HIO3,
故答案为:5Cl2+I2+6H2O═10HCl+2HIO3;
(2)①甲为原电池装置,铁作负极,负极反应为Fe-2e-═Fe2+,故答案为:Fe-2e-═Fe2+;
②由2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+2H2SO4,要使溶液恢复原状态,可加入CuO(或CuCO3),一段时间后溶液的pH变为1,则c(H+)=0.1mol/L-10-5mol/L=0.1mol/L,n(H+)=0.2L×0.1mol/L=0.02mol,则由电解反应可知析出的Cu的物质的量为0.01mol,由Cu原子守恒可知,m(CuO)=0.01mol×80g/mol=0.8g,或m(CuCO3)=0.01mol×124g/mol=1.24g,
故答案为:CuO(或CuCO3);0.8(或1.24).
点评 本题考查原电池与电解池的工作原理,明确离子放电顺序、电极反应式的书写即可解答,难度不大.

 53随堂测系列答案
53随堂测系列答案| A. | 甲烷 | B. | 石墨 | C. | 晶体硅 | D. | 水晶 |
| A. | 沸点:NH3>AsH3>PH3 | B. | 熔点:Cs>Li>Na | ||
| C. | 酸性:HClO4>H2SO4>H3PO4 | D. | 碱性:NaOH>Mg(OH)2>Al(OH)3 |
| A. | 硅的提纯与应用,促进了半导体元件与集成芯片的发展 | |
| B. | 水泥、玻璃、塑料都是高分子材料 | |
| C. | 钢化玻璃与普通玻璃的主要成分不同 | |
| D. | 通常情况下,铝合金在空气中不易被腐蚀,可用做建筑材料 |
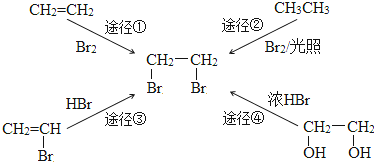
| A. | 途径① | B. | 途径② | C. | 途径③ | D. | 途径④ |
| A. | 3 | B. | 6 | C. | 9 | D. | 12 |

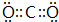 ;
; ;
; 如图所示,是原电池的装置图.请回答:
如图所示,是原电池的装置图.请回答: