题目内容
2.下列实验装置或操作与粒子的大小无直接关系的是( )| A. | 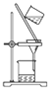 过滤 | B. | 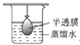 渗析 | C. | 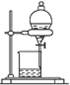 分液 | D. | 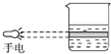 丁达尔效应 |
分析 A.过滤中不溶性固体不能透过滤纸;
B.渗析中胶体不能透过半透膜;
C.分液与物质的溶解性有关;
D.分散系中分散质粒子直径在1nm~100nm之间的具有丁达尔现象.
解答 解:A.悬浊液的分散质粒子不能通过滤纸,过滤利用了分散质粒子的大小进行分离,故A不选;
B.胶体的分散质粒子不能透过半透膜,溶液的分散质粒子能透过半透膜,渗析利用了分散质粒子的大小进行分离,故B不选;
C.分液与物质的溶解性有关,分层液体可利用分液法分离,与物质微粒大小无直接关系,故C选;
D.胶体微粒能对光线散射,产生丁达尔效应,而溶液中的离子很小,不能产生丁达尔效应,丁达尔效应与分散质粒子的大小有关,故D不选;
故选C.
点评 本题考查混合物的分离提纯,为高频考点,把握混合物分离原理及实验装置为解答的关键,侧重分析与应用能力的考查,注意分液与溶解性有关,题目难度不大.

练习册系列答案
相关题目
13.已知反应A+B?C+D的能量变化如图所示,下列说法正确的是( )
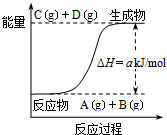

| A. | 该体系的压强不变时标志此反应处于平衡状态 | |
| B. | 若该反应中有电子得失,则可设计成原电池 | |
| C. | 反应物的总键能高于生成物的总键能 | |
| D. | 该反应中的反应物A和B的转化率一定相同 |
13.关于下列各实验装置的叙述中,不正确的是( )


| A. | 装置①可用于分离酒精和水的混合物 | |
| B. | 装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体 | |
| C. | 装置②中若装满水,收集H2的时候应该从a口通入H2 | |
| D. | 装置①用CCl4萃取碘水中的碘时,CCl4层在下层 |
14. 某同学设计了一个测定溶液导电性的实验(如图所示):他先测10.0ml 0.10mol/L H2SO4溶液的导电能力,然后在其中慢慢滴加15.0ml 0.10mol/L Ba(OH)2溶液,并不断搅拌.知溶液中的离子浓度与Ba(OH)2溶液的体积关系如下:
某同学设计了一个测定溶液导电性的实验(如图所示):他先测10.0ml 0.10mol/L H2SO4溶液的导电能力,然后在其中慢慢滴加15.0ml 0.10mol/L Ba(OH)2溶液,并不断搅拌.知溶液中的离子浓度与Ba(OH)2溶液的体积关系如下:
请根据上述题意,回答下列问题:
(1)可观察到的现象为灯泡由亮到暗到灭再到亮,溶液中有白色沉淀产生;当15.0ml 0.10mol/L Ba(OH)2溶液全部滴入H2SO4溶液中后,反应的离子方程式SO42-+2H++Ba2++2OH-═BaSO4↓+2H2O.
(2)有关该实验现象的说法正确的是A
A.溶液的导电性与溶液中自由移动的离子浓度有关
B.灯泡最暗时溶液中自由移动离子的浓度为零
C.往盐酸和硫酸溶液中滴加氢氧化钡溶液时现象相同.
(3)下列物质是该实验中的反应物和生成物,其中属于弱电解质的是D
A.H2SO4 B.Ba(OH)2 C.BaSO4 D.H2O.
 某同学设计了一个测定溶液导电性的实验(如图所示):他先测10.0ml 0.10mol/L H2SO4溶液的导电能力,然后在其中慢慢滴加15.0ml 0.10mol/L Ba(OH)2溶液,并不断搅拌.知溶液中的离子浓度与Ba(OH)2溶液的体积关系如下:
某同学设计了一个测定溶液导电性的实验(如图所示):他先测10.0ml 0.10mol/L H2SO4溶液的导电能力,然后在其中慢慢滴加15.0ml 0.10mol/L Ba(OH)2溶液,并不断搅拌.知溶液中的离子浓度与Ba(OH)2溶液的体积关系如下:| Ba(OH)2(ml) | 溶液中的总离子浓度(mol/L) |
| 0.0 | 0.30 |
| 5.0 | 0.10 |
| 10.0 | ≈0.00 |
| 15.0 | 0.06 |
(1)可观察到的现象为灯泡由亮到暗到灭再到亮,溶液中有白色沉淀产生;当15.0ml 0.10mol/L Ba(OH)2溶液全部滴入H2SO4溶液中后,反应的离子方程式SO42-+2H++Ba2++2OH-═BaSO4↓+2H2O.
(2)有关该实验现象的说法正确的是A
A.溶液的导电性与溶液中自由移动的离子浓度有关
B.灯泡最暗时溶液中自由移动离子的浓度为零
C.往盐酸和硫酸溶液中滴加氢氧化钡溶液时现象相同.
(3)下列物质是该实验中的反应物和生成物,其中属于弱电解质的是D
A.H2SO4 B.Ba(OH)2 C.BaSO4 D.H2O.
12.下列说法正确的是( )
| A. | 氯气溶于水的离子方程式:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 向含I-的无色溶液中滴加少量新制氯水,再滴加淀粉溶液,若溶液变成蓝色,则氧化性:Cl2>I2 | |
| C. | 为测定新制氯水的pH,用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡对照即可 | |
| D. | 漂白粉在空气中久置变质是因为漂白粉中的CaCl2与空气中的CO2反应生成CaCO3 |
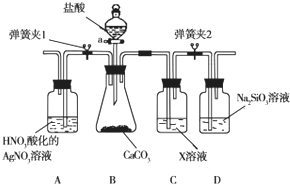 某同学为了验证碳和硅两种元素非金属性的相对强弱,用如图所示装置进行实验(夹持仪器已略去,气密性已检验).
某同学为了验证碳和硅两种元素非金属性的相对强弱,用如图所示装置进行实验(夹持仪器已略去,气密性已检验).