题目内容
17.下列实验现象与氧化还原反应有关的是( )| A. | NH3使湿润的红色石蕊试纸变蓝 | |
| B. | 向硅酸钠溶液中滴加适量稀盐酸,有透明的凝胶形成 | |
| C. | 将氯水长期放置,黄绿色消失 | |
| D. | 向Fe2(SO4)3溶液中滴加NaOH溶液,生成红褐色沉淀 |
分析 氧化还原反应的特征是元素化合价的升降,结合物质的性质以及反应的特点,判断元素的化合价是否发生变化,可判断反应是否属于氧化还原反应,以此解答.
解答 解:A.氨气与水反应生成一水合氨,一水合氨发生电离,溶液呈碱性,没有发生氧化还原反应,故A不选;
B.硅酸钠与盐酸发生复分解反应生成硅酸,没有发生氧化还原反应,故B不选;
C.Cl2+H2O=HCl+HClO,该反应中Cl元素化合价由0价变为+1价、-1价,所以有电子转移,属于氧化还原反应,故C选;
D.向Fe2(SO4)3溶液中滴加NaOH溶液,生成红褐色沉淀,发生复分解反应,没有元素化合价的变化,不是氧化还原反应,故D不选.
故选C.
点评 本题考查氧化还原反应,侧重考查基本理论,明确氧化还原反应的本质以及特征即可解答,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.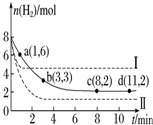 将6mol CO2和8mol H2充入一容积为2L的密闭容器中(温度保持不变)发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0测得H2的物质的量随时间变化如右图中实线所示(图中字母后的数字表示对应的坐标).该反应在8~10min内CO2的平均反应速率是( )
将6mol CO2和8mol H2充入一容积为2L的密闭容器中(温度保持不变)发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0测得H2的物质的量随时间变化如右图中实线所示(图中字母后的数字表示对应的坐标).该反应在8~10min内CO2的平均反应速率是( )
 将6mol CO2和8mol H2充入一容积为2L的密闭容器中(温度保持不变)发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0测得H2的物质的量随时间变化如右图中实线所示(图中字母后的数字表示对应的坐标).该反应在8~10min内CO2的平均反应速率是( )
将6mol CO2和8mol H2充入一容积为2L的密闭容器中(温度保持不变)发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0测得H2的物质的量随时间变化如右图中实线所示(图中字母后的数字表示对应的坐标).该反应在8~10min内CO2的平均反应速率是( )| A. | 0.5mol•L-1•min-1. | B. | 0.1mol•L-1•min-1 | ||
| C. | 0 mol•L-1•min-1 | D. | 0.125mol•L-1•min-1 |
5.下列各项操作中,不发生“先产生沉淀,后沉淀溶解”现象的是( )
①向硅酸钠溶液中通入过量的CO2②向Fe(OH)3胶体中逐滴加入过量的稀盐酸
③向NaAlO2溶液中通入过量的CO2 ④向澄清石灰水中通入缓慢过量的CO2.
①向硅酸钠溶液中通入过量的CO2②向Fe(OH)3胶体中逐滴加入过量的稀盐酸
③向NaAlO2溶液中通入过量的CO2 ④向澄清石灰水中通入缓慢过量的CO2.
| A. | ①② | B. | ①③ | C. | ①④ | D. | ②③ |
2.下列物质的体积约为22.4L的是( )
| A. | 标准状况下1molH2O | |
| B. | 20℃、101kPa时36.5gHCl | |
| C. | 常温常压下17gNH3 | |
| D. | 标准状况下0.4mol H2和0.6molO2的混合气 |
9.下列括号中的物质是去除杂质所用的试剂,其中错误的是( )
| A. | CaO中有少量CaCO3(盐酸) | |
| B. | 氢气中含有少量氯化氢(苛性钠溶液) | |
| C. | 硫酸亚铁溶液中含有少量硫酸铜(铁粉) | |
| D. | CO2中有少量CO(灼热的氧化铜) |
6.已知某有机物含有4个C,每个碳原子都以键长相等的三条单键连接3个C,且整个结构中所有碳碳键之间的夹角都为60°,则下列说法不正确的是( )
| A. | 该有机物不存在 | B. | 该有机物的分子式为C4H4 | ||
| C. | 该有机物的空间构型为正四面体 | D. | 该有机物不属于笨的同系物 |