题目内容
14.NA表示阿伏加德罗常数的值,下列说法正确的是( )| A. | 标准状况下,22.4 L二氯甲烷的分子数约为NA个 | |
| B. | 盛有SO2的密闭容器中含有NA个氧原子,则SO2的物质的量为0.5 mol | |
| C. | 17.6g丙烷中所含的极性共价键为4NA个 | |
| D. | 1molFeI2与足量氯气反应时转移的电子数为2NA |
分析 A、标况下二氯甲烷为液体;
B、1mol二氧化硫中含2mol氧原子;
C、求出丙烷的物质的量,然后根据丙烷中含8条极性共价键来分析;
D、1molFeI2与足量氯气反应时消耗1.5mol氯气.
解答 解:A、标况下二氯甲烷为液体,故不能根据气体摩尔体积来计算其物质的量和分子个数,故A错误;
B、1mol二氧化硫中含2mol氧原子,故当含NA个氧原子时,二氧化硫的分子个数为0.5NA个,物质的量为0.5mol,故B正确;
C、17.6g丙烷的物质的量为0.4mol,而丙烷中含8条极性共价键,故0.4mol丙烷中含3.2NA条极性共价键,故C错误;
D、1molFeI2与足量氯气反应时消耗1.5mol氯气,而氯气反应后变为-1价,故转移3NA个电子,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
相关题目
2.下列离子方程式书写正确的是( )
| A. | 钠与水的反应:Na+H2O=Na++OH-+H2↑ | |
| B. | 碳酸钙溶于稀醋酸:CaCO3+2H +=Ca2++H2O+CO2↑ | |
| C. | 氢氧化钠溶液中通入过量二氧化碳:OH-+CO2=HCO3- | |
| D. | 向碳酸氢铵稀溶液中加入过量烧碱溶液:NH4++OH-=NH3•H2O |
9.下列化学性质中,甲苯不具备的是( )
| A. | 能使溴水褪色发生加成反应 | B. | 可以在空气中燃烧 | ||
| C. | 与Cl2发生取代反应 | D. | 能使酸性KMnO4溶液褪色 |
19.下列不存在丁达尔效应的分散系是( )
| A. | 雾 | B. | 淀粉溶液 | C. | 食盐水 | D. | 氢氧化铁胶体 |
3.关于硫和氧的性质叙述正确的是( )
| A. | 硫在O2中燃烧生成SO2 | B. | 硫在O2中燃烧生成SO3 | ||
| C. | 硫的非金属性比氧的强 | D. | 氧、硫均只有氧化性 |
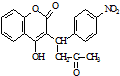
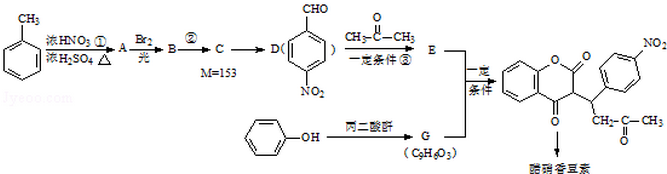 已知:R1-CHO
已知:R1-CHO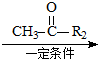 R1-CH=
R1-CH= +H2O
+H2O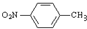 ;反应②的反应类型取代反应.
;反应②的反应类型取代反应.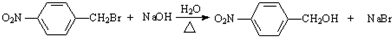 .
.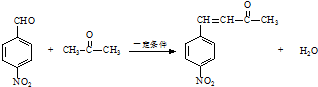 .
.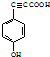 .
.